Ingin mempelajari materi kimia, khususnya tentang Titrasi Lanjutan (Kompleksometri)? Supaya lebih paham, kamu bisa menyimak pembelajarannya di sini. Kamu juga bisa mengerjakan soal latihan untuk mempraktikkan materi yang telah dijelaskan.
Lewat pembahasan ini, kamu bisa belajar mengenai Titrasi Lanjutan (Kompleksometri). Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Titrasi Lanjutan (Kompleksometri) dalam bentuk pdf pada link dibawah ini:
Definisi
Pengertian titrasi adalah suatu metode penentuan konsentrasi zat dengan cara mereaksikan larutan tersebut dengan larutan yang sudah diketahui konsentrasinya secara bertahap (tetes demi tetes).
1. Titrasi Asam Basa
Untuk proses analisis konsentrasi suatu larutan, titrasi adalah salah satu cara yang paling mudah dan akurat. Titrasi pada intinya adalah proses penentuan konsentrasi suatu larutan dengan mereaksikan larutan yang sudah tertentu konsentrasinya (larutan standar).
Pada titrasi asam basa digunakan reaksi penetralan dengan mengukur volume dari asam atau basa yang bereaksi sehingga proses ini disebut juga titrasi volumetri.
Istilah-Istilah Penting pada Proses Titrasi
Berikut ini istilah-istilah yang penting pada proses titrasi:
1. Zat peniter
Zat peniter : larutan standar yang telah diketahui konsentrasinya, terbagi ke dalam
(a) primer : ketelitian tinggi, contoh: KHF (Kalium Hidrogen Ftalat)
(b) sekunder: kemolarannya ditentukan dengan larutan standar primer
2. Titik Ekivalen (TE)
Titik Ekivalen (TE) : pH pada saat asam dan basa tepat habis bereaksi
konsentrasi ekivalen dapat dihitung:
$V_{A}\times M_{A}\times n_{A}=V_{B}\times M_{B}\times n_{B}$
dimana,
$V_{A}=$ volume asam
$M_{A}=$ konsentrasi asam
$n_{A}=$ valensi asam
$V_{B}=$ volume basa
$M_{B}=$ konsentrasi basa
$n_{B}=$ valensi basa
3. Titik Akhir (TA)
Titik Akhir (TA) : pH pada saat indikator berubah warna.
Cara atau metode titrasi:
- Larutan yang akan diteteskan dimasukkan ke dalam buret (pipa panjang berskala), inilah yang disebut peniter
- Larutan yang akan dititrasi dimasukkan ke dalam erlenmeyer dengan mengukur volumenya terlebih dahulu memakai pipet volume
- Memberikan beberapa tetes indikator pada larutan yang dititrasi, pilih indikator dengan perubahan warna sekitar TE.
- Lakukan titrasi, yaitu larutan yang berada dalam buret diteteskan perlahan-lahan melalui keran ke dalam erlenmeyer sambil digoyang agar merata. Penambahan peniter dihentikan ketika sudah terjadi perubahan warna yang tidak hilang ketika larutan digoyangkan, yang menandakan telah tercapai TA.
- Mencatat volume yang dibutuhkan peniter dengan melihat volume yang berkurang pada buret setelah titrasi.
Membuat Kurva Titrasi
1. Titrasi asam kuat oleh basa kuat dan sebaliknya
pH ekivalen adalah 7, sehingga kurva yang akan didapat:
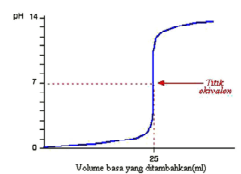
Bila dilakukan titrasi sebaliknya maka bentuk kurva dibalik menghadap kiri (mulai dari pH tinggi)
2. Titrasi asam kuat oleh basa lemah dan sebaliknya
pH ekivalen di bawah 7, sehingga bentuk kurvanya:
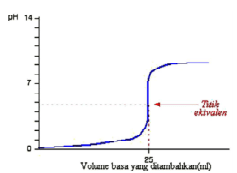
Bila dilakukan titrasi sebaliknya (basa lemah oleh asam kuat) maka kurva dibalik menghadap kiri
3. Titrasi asam lemah oleh basa kuat dan sebaliknya
pH ekivalen di atas 7, sehingga kurvanya:
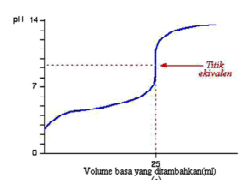
Bila dilakukan titrasi sebaliknya (basa kuat oleh asam kuat) maka kurva dibalik menghadap kiri.
2. Titrasi Balik
Suatu titrasi secara umum dilakukan secara langsung, akan tetapi apabila suatu reaksi berlangsung lambat dan tidak dapat diperoleh titik akhir yang tegas. Maka kita gunakan metode titrasi balik untuk mengatasinya.
Pada metode titrasi balik ini, penentuan konsentrasi analit (zat yang ingin dianalisis) dalam sampel dilakukan dengan cara menambahkan senyawa berlebih yang diketahui konsentrasinya, kemudian kelebihan senyawa yang tidak bereaksi dengan analit dititrasi balik dengan peniter yang tepat. Bila digambarkan dalam diagram seperti ini:
Bila A adalah analit, $A+B\rightarrow$C + kelebihan B, kelebihan B + D $\rightarrow$ hasil reaksi. Dari nilai kelebihan B yang bereaksi dengan D inilah kita dapatkan konsentrasi analit.
Sehingga didapat:
konsentrasi peniter D = konsentrasi B berlebih. konsentrasi A = konsentrasi B yang digunakan – konsentrasi B berlebih
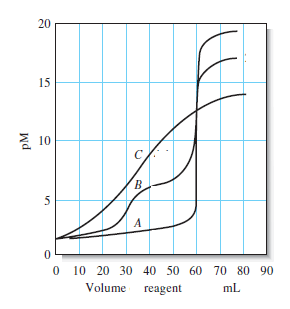
3 Titrasi Kompleksometri
Titrasi kompleksometri adalah jenis titrasi yang dilakukan berdasarkan pembentukan senyawa kompleks dimana reaksi antara bahan yang dianalisis dan titrat akan membentuk suatu senyawa kompleks.
Senyawa kompleks yang dimaksud di sini adalah senyawa kompleks yang dibentuk melalui reaksi ion logam, sebuah kation seperti ion kalsium, $\mbox{Ca}^{2+}$, dengan sebuah anion seperti ion sianida dan yang lebih sering digunakan saat ini adalah EDTA (etilendiamin tetraacetic acid). Faktor-faktor yang membuat EDTA baik sebagai pereaksi titrimetri antara lain:
- Selalu membentuk kompleks ketika direaksikan dengan ion logam
- Kestabilannya dalam membentuk kelat sangat konstan sehingga reaksi berjalan sempurna (kecuali dengan logam alkali),
- Dapat bereaksi cepat dengan banyak jenis ion logam
- Telah dikembangkan indikatornya secara khusus
- Mudah diperoleh bahan baku primernya
- Dapat digunakan baik sebagai bahan yang dianalisis maupun sebagai bahan untuk standardisasi.
Salah satu aplikasi titrasi ini adalah untuk menentukan kesadahan air. EDTA (ethylene diamine tetraacetic) merupakan suatu kompleks kelat yang larut ketika ditambahkan ke dalam suatu larutan yang mengandung kation logam tertentu seperti $\mbox{Ca}^{2+}$ dan $\mbox{Mg}^{2+}$, di mana akan membentuk kompleks dengan logam-logam tersebut.
Ketika ditambahkan suatu indikator EBT ke dalam larutan yang mengandung kompleks tersebut maka akan menghasilkan perbahan warna pada pH tertentu, sehingga dengan prinsip ini nilai kesadahan air dapat dianalisis.
Pertama indikator akan membentuk kompleks dengan ion kalsium yang menghasilkan larurtan berwarna merah:
1) $\mbox{H}_{2}\mbox{In}^{-}+\mbox{Ca}^{2+}\rightarrow\mbox{CaIn}^{-}+\mbox{2H}^{+}$
Pada titik akhir, EDTA akan kompleks dengan kalsium dan indikator menjadi lepas, yaitu ditandai oleh warna merah berganti warna biru:
2) $\mbox{EDTA + CaIn}^{-}+\mbox{2H}^{+}\rightarrow\mbox{H}_{2}\mbox{In}^{-}+\mbox{CaEDTA}$
Contoh Soal Titrasi Lanjutan (Kompleksometri) dan Pembahasan
1. Pada suatu proses titrasi, 20 mL HCl sebagai sampel diencerkan hingga volumenya tepat 100 mL. Sebanyak 10 mL dari larutan tersebut diambil dan dititrasi dengan KOH 0,1 M. Dari hasil eksperimen ditemukan bahwa peniter berkurang sebanyak 20 mL. Tentukan konsentrasi sampel awal!
Jawaban
Pertama-tama kita hitung konsentrasi HCl yang dititrasi:
$\begin{aligned}V_{A}\times M_{A}\times n_{A} & =V_{B}\times M_{B}\times n_{B}\\ 10\times M_{A}\times1 & =20\times0,1M\times1\\ M_{A} & =0,2M \end{aligned} $
Ini adalah konsentrasi setelah pengenceran, maka konsentrasi sebelum pengenceran:
$\begin{aligned}V_{1}M_{1} & =V_{2}M_{2}\\ 20\times M_{1} & =100\times0,2M\\ M_{1} & =1M \end{aligned} $.
2. Suatu sampel 0,500 g yang mengandung $Na_{2}CO_{3}$ dianalisis menggunakan metode titrasi balik dimana pertama-tama ditambahkan 50 mL 0,100 M HCl , dididihkan untuk menghilangkan $CO_{2}$ kemudian dititrasi balik dengan 0,100 M NaOH. Jika diperlukan 5,6 mL NaOH untuk titrasi balik, berapa persen $Na_{2}CO_{3}$ dalam sampel?
Jawaban
Kita mulai dari reaksi titrasi balik:
$NaOH+HCl\rightarrow NaCl+H_{2}O$
sehingga,
$\begin{aligned}mol\, HCl\, lebih & =mol\, NaOH\\ & =0,1\times5,6\, mmol\\ & =0,56\, mmol \end{aligned} $
Reaksi awal adalah:
$Na_{2}CO_{3}+2HCl\rightarrow2NaCl+CO_{2}+H_{2}O$
Maka, mol $Na_{2}CO_{3}=0,5\times HCl\, bereaksi$
$\begin{aligned}mol\, Na_{2}CO_{3} & =0,5\times(50\times0,1-0,56)mmol\\ & =2,22\, mmol\\ mNa_{2}CO_{3} & =2,22\times106\, mg\\ & =235,32mg \end{aligned} $
Sehingga persentasenya di dalam sampel:
$\frac{235,32}{500}\times100\%=47,064\%$