Kalau kamu ingin belajar Sifat Fisis Senyawa secara lebih mendalam, coba simak penjelasan yang ada di sini. Setelah menerima materi, kamu bisa langsung mempraktikkannya dengan mengerjakan latihan soal yang telah kami sediakan.
Lewat pembahasan ini, kamu bisa belajar mengenai Sifat Fisis Senyawa. kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Oleh karenanya, pembahasan ini bisa langsung kamu praktikkan. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Sifat Fisis Senyawa dalam bentuk pdf pada link dibawah ini:
Definisi
Sifat dari suatu senyawa yang dapat diamati atau diukur tanpa mengubah identitas kimia senyawa tersebut.
Sifat Fisis Senyawa
Berikut ini beberapa sifat fisis yang dipengaruhi oleh jenis ikatan yang dimiliki oleh suatu senyawa.
1. Titik Didih
Secara umum, senyawa ion mempunyai titik didih lebih tinggi dari kovalen. Titik didih berkaitan dengan gaya tarik-menarik antar partikel (kohesi). Jadi ada hubungan yang semakin kuat maka semakin tinggi titik didihnya. Gaya tarik antar ion pada umumnya lebih kuat daripada gaya tarik antar molekul non-ion.
2. Volatilitas atau kemudahan
Volatilitas atau kemudahan menguap pun dipengaruhi oleh kekuatan gaya tarik-menarik antar partikelnya. Sehingga secara umum pun senyawa kovalen lebih mudah menguap dari senyawa ionik.
3. Kelarutan
Senyawa ion cenderung mudah larut dalam air namun sulit larut dalam pelarut organik (eter, aseton dan lainnya). Sebaliknya senyawa kovalen harus dilihat sifatnya, apabila polar maka mudah larut dalam air sementara senyawa nonpolar mudah larut dalam pelarut organik
4. Daya hantar listrik.
Kemampuan menghantarkan listrik dipengaruhi keberadaan elektron bebas dan ion bebas. Jika terdapat ion bebas atau elektron bebas, makan zat tersebut dapat menghantarkan listrik. Senyawa ion padat tidak menghantar lsitrik, tetapi lelehannya dapat karena adanya ion yang bergerak bebas.
Sementara itu senyawa kovalen tidak dapat menghantarkan listrik baik dalam wujud padatan maupun lelehan. Dalam wujud larutan senyawa ionik dan kovalen polar umumnya mampu menghantarkan listrik. Namun ada senyawa kovalen yang dapat menghantarkan listrik contohnya grafit karena adanya elektron yang bergerak bebas.
Sifat fisis senyawa berdasarkan jenis ikatannya
Selain itu untuk unsur-unsur atau paduan logam (amalgam) yang memiliki ikatan logam, cenderung akan memiliki sifat fisis sebagai berikut: titik leleh dan titik didih cenderung tinggi, tidak larut dalam air maupun pelarut organik (hanya larut pada beberapa asam kuat), volatilitas rendah, dapat menghantarkan listrik pada fase padat maupun lelehan, tidak pada larutan.
Bila disimpulkan perbedaan sifat fisis senyawa berdasarkan jenis ikatannya adalah
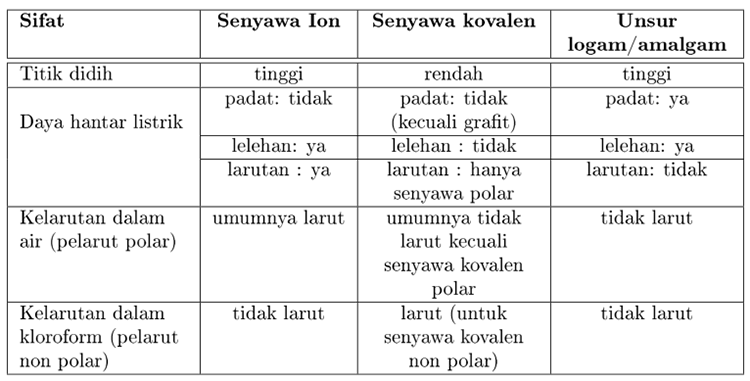
Contoh Soal Sifat Fisis Senyawa dan Pembahasannya
- Deterjen diketahui adalah suatu senyawa ionik, meski demikian mengapa kita dapat mencium aroma yang kuat?
Jawaban
Pada deterjen ditambahkan banyak senyawa aditif (tambahan) lainnya, terutama wewangian yang tergolong senyawa molekuler/kovalen yang mudah menguap sehingga dapat tercium dengan jelas. - Perhatikan tabel berikut yang berisi berbagai sifat fisis untuk 5 zat yang belum diketahui,

a. Di antara kelima zat itu, manakah yang merupakan senyawa ion dan manakah kovalen? Jelaskan
b. Senyawa manakah yang akan memiliki kelarutan paling tinggi di dalam heksana?
Jawaban- Untuk pertanyaan (a):
- Senyawa L
Titik leleh dan titik didih relatif tinggi, kelarutan di air buruk, daya hantar baik pada padatan maupun lelehan, sehingga bukan merupakan senyawa kovalen maupun ionik, kemungkinan suatu unsur logam - Senyawa M
Titik leleh dan titik didih relatif sedang, tidak larut dalam air, serta tidak dapat menghantarkan listrik baik pada wujud padat maupun lelehannya. Kemungkinan adalah suatu senyawa kovalen non-polar - Senyawa N
Titik leleh relatif rendah sementara titik didih relatif sedang, tidak larut dalam air, dapat menghantarkan listrik baik pada fase padat maupun lelehan. Kemungkinan adalah suatu unsur logam - Senyawa O
Titik leleh dan titik didih relatif tinggi, larut di air, daya hantar baik pada lelehan. Kemungkinan adalah senyawa ionik - Senyawa P
Titik leleh dan titik didih realtif rendah, tidak larut di air daya hantarnya buruk baik pada padatan maupun lelehan. Kemungkinan senyawa kovalen non polar
- Senyawa L
- Senyawa kovalen non polar akan memiliki kelarutan paling tinggi di dalam heksana (yang juga non polar) sehingga kemungkinan senyawa M dan P dapat larut.
Meski demikian, melihat titik leleh dan titik didih P yang lebih rendah, akan memiliki kemiripan sifat yang lebih besar lagi dengan heksana (gaya intermolekul lemah).
Sehingga P adalah senyawa yang diperkirakan akan memiliki kelarutan paling tinggi di dalam heksana.
- Untuk pertanyaan (a):




