Ingin mempelajari teori Sifat Koligatif Larutan secara lebih mendalam? Tertarik juga untuk mengerjakan soal latihan terkait materi ini? Kamu bisa mendapatkan penjelasan materi beserta soal latihannya di sini. Yuk, langsung saja disimak!
Lewat pembahasan ini, kamu bisa belajar mengenai Sifat Koligatif Larutan. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Sifat Koligatif Larutan dalam bentuk pdf pada link dibawah ini:
Kenaikan Titik Didih dan Penurunan Titik Beku
Untuk memahami konsep kenaikan titik didih larutan kita akan contoh dalam kehidupan sehari-hari yakni apabila ke dalam air dilarutkan suatu zat tertentu, seperti yang kita ketahui akan terjadi penurunan tekanan uap larutan, sehingga pada suhu $\mbox{100}^{\circ}\mbox{C}$ larutan air belum mendidih karena tekanan uapnya belum mencapai 760 mmHg.
Untuk mencapai tekanan uap 760 mmHg maka perlu dipanaskan lebih tinggi lagi akibatnya larutan mendidih pada suhu lebih dari $\mbox{100}^{\circ}\mbox{C}$.
Ini berarti bahwa titik didih larutan lebih tinggi daripada titik didih pelarut murninya. Selisih antara titik didih larutan dengan titik didih pelarut murni disebut kenaikan titik didih ( $\Delta Tb)$.
$\Delta T_{b}=T_{b}-T_{b}^{\circ}$
dimana
$\Delta T_{b}$: kenaikan titik didih,
$T_{b}$: titik didih larutan,
$T_{b}^{\circ}$: titik didih pelarut murni
Untuk memudahkan kamu belajar, kamu dapat download kenaikan titik didih pdf pada link di awal halaman ini.
Demikian pula pada penurunan titik beku larutan, tekanan uap larutan juga lebih rendah daripada tekanan uap pelarut murni. Sehingga agar larutan membeku, harus didinginkan ke suhu yang lebih rendah akibatnya titik beku larutan lebih rendah dari titik beku pelarut murni.
Jadi penyebab penurunan titik beku karena tekanan uap larutan lebih rendah daripada tekanan uap pelarut murni.
Untuk mempelajari lebih lanjut kamu dapat download penurunan titik beku pdf pada link awal halaman ini. Selanjutnya perubahan temperatur titik beku ini disebut penurunan titik beku larutan ( $\Delta T_{f}$).
$\Delta T_{f}=T_{f}^{\circ}-T_{f}$
dimana
$\Delta T_{f}$: penurunan titik beku,
$T_{f}$: titik beku larutan,
$T_{f}^{\circ}$: titik beku pelarut murni
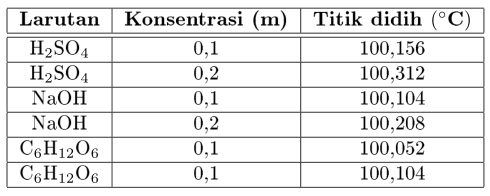
Pada larutan encer, kenaikan titik didih dan penurunan titik beku berbanding lurus dengan konsentrasi molal larutan.
$\Delta T_{b}=K_{b}\times m$ dan $\Delta T_{f}=K_{f}\times m$
dimana:
$\Delta T_{b}$= kenaikan titik didih
m = molalitas
$K_{b}$= kenaikan titik didih molal pelarut
$\Delta T_{f}$= penurunan titik beku
$K_{f}$= penurunan titik beku molal pelarut
Jadi, pengaruh zat terlarut yang tidak mudah menguap adalah menurunkan tekanan uap, menaikkan titik didih, dan menurunkan titik beku.

Untuk kenaikan titik didih dan penurunan titik beku untuk larutan elektrolit perlu diperhitungkan faktor van’t hoff sebagai berikut: sebagai berikut:
$\Delta T_{b}=K_{b}\times m\times i$ dan $\Delta T_{f}=K_{f}\times m\times i$
Tekanan Osmotik
Pengertian tekanan osmotik adalah tekanan yang diperlukan untuk mencegah terjadinya osmosis. Di awal halaman ini kamu dapat download tekanan osmotik pdf sehingga bisa memudahkan kamu dlm belajar.
Bila dua larutan yang konsentrasinya berbeda, yang satu pekat dan yang lainnya encer dipisahkan oleh membran semipermiabel, maka molekul-molekul pelarut akan mengalir dari larutan yang lebih encer ke larutan yang lebih pekat, sedangkan molekul zat terlarut tidak mengalir.
Hal ini terjadi karena partikel pelarut lebih kecil daripada partikel zat terlarut sehingga partikel pelarut dapat menembus membran semipermiabel dan partikel zat terlarut tidak.
Aliran suatu pelarut dari suatu larutan dengan konsentrasi lebih rendah ke larutan dengan konsentrasi tinggi melalui membran semipermiabel disebut osmosis.
Peristiwa osmosis dapat dicegah dengan memberi tekanan pada permukaan larutan. Tekanan yang diperlukan untuk mencegah terjadinya osmosis ini disebut tekanan osmotik.

Tekanan osmotik bergantung pada konsentrasi dan bukan pada jenis partikel zat terlarut. Menurut Van’t Hoff, tekanan osmotik larutan encer dapat dihitung dengan rumus yang serupa dengan persamaan gas ideal.
$\begin{alignedat}{1}PV & =nRT\\
\pi V & =nRT\\
\pi & =\frac{nRT}{V}\\
\pi & =M\cdot R\cdot T
\end{alignedat}
$
Keterangan :
$\pi$ = tekanan osmotik (atm)
V = volume larutan (liter)
R = tetapan gas (0,082 L atm/mol K)
T = suhu mutlak (K)
Untuk tekanan osmotik untuk larutan elektrolit juga diperhitungkan faktor Van’t Hoff sebagai berikut:
$\pi=M\cdot R\cdot T\cdot i$
Contoh Soal Sifat Koligatif Larutan dan Pembahasannya
- Suatu larutan dibuat dengan cara melarutkan 6 gram urea $\mbox{CO(NH}{}_{2})_{2}$ dalam 500 gram air. ($K_{b}$ air= 0,52 \textdegree{}C/m, $K_{f}$ air = 1,86 ºC/m , Ar C = 12, O = 16, N = 14, H = 1). Tentukan titik didih dan titik beku larutan!
Jawaban- Titik didih larutan, urea merupakan senyawa non elektrolit, sehingga tidak digunakan $i$Jawaban
$\begin{alignedat}{1}\Delta T_{b} & =K_{b}\times m\\
& =0,52\times\frac{6}{60}\times\frac{1000}{500}\\
& =0,104\\
T_{b} & =T_{b}^{\circ}+\Delta T_{b}\\
& =100+0,104\\
& =100,104^{\circ}C
\end{alignedat}
$ - Titik beku larutan, urea merupakan senyawa non elektrolit, sehingga tidak digunakan $i$
$\begin{alignedat}{1}\Delta T_{f} & =K_{f}\times m\\
& =1,86\times\frac{6}{60}\times\frac{1000}{500}\\
& =0,372\\
T_{f} & =T_{f}^{\circ}-\Delta T_{f}\\
& =0-0,372\\
& =-0,372^{\circ}C
\end{alignedat}
$
–
- Titik didih larutan, urea merupakan senyawa non elektrolit, sehingga tidak digunakan $i$Jawaban
- Sebanyak 2,34 gram NaCl dilarutkan dalam air sampai volume larutan 500 mL pada suhu $27^{\circ}C$. Hitunglah tekanan osmotik larutan tersebut.
Jawaban
Larutan NaCl merupakan larutan elektrolit kuat dengan $\alpha=1$,
$NaCl\rightarrow Na^{+}+Cl^{-}$
$\begin{alignedat}{1}i & =(n-1)+1\\|
& =(2-1)+1\\
& =2\\
\pi & =M\cdot R\cdot T\cdot i\\
& =\frac{2,34}{58,5}\times\frac{1000}{500}\times(27+273)\times2\\
& =48\, atm
\end{alignedat}
$