Koloid merupakan salah satu materi kimia yang cukup menarik untuk dibahas. Kalau kebetulan kamu ingin belajar tentang materi ini lebih dalam, simak penjelasan lengkapnya berikut. Kami juga telah menyediakan soal latihan yang bisa dikerjakan untuk mengasah kemampuanmu.
Lewat pembahasan ini, kamu bisa belajar mengenai Koloid. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal dalam bentuk pdf pada link dibawah ini:
Definisi
Pengertian materi koloid (colloid) adalah zat yang berpencar dalam zat pelarut sebagai butir yang lebih besar daripada molekul, tetapi tidak dapat dilihat dengan mata (harus dengan mikroskop). Contoh dalam kehidupan sehari hari yang mudah dijumpai adalah susu, sampo dan sabun cair.
Konsep Dasar
Suatu campuran dapat dibedakan menjadi campuran homogen (larutan), heterogen (suspensi) dan koloid sesuai dengan ukuran partikel zat terlarutnya. Perbedaan ketiganya dapat dirangkum sebagai berikut

Jenis-jenisnya dapat dirangkum sebagai berikut sesuai fase terdispersi dan pendispersinya berikut ini:

Selain itu dapat pula digolongkan berdasarkan interaksi dengan medium pendispersinya, menjadi koloid liofil dan liofob
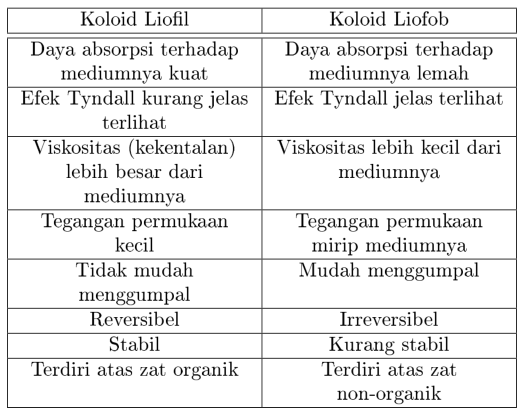
Sistem Koloid
Suatu sistem colloid memiliki sifat khas sebagai berikut:
1. Efek Tyndall
Efek Tyndall adalah peristiwa penghamburan cahaya oleh partikel-partikel sehingga tampak lintasan berkas sinar tersebut. Peristiwa ini terjadi karena ukuran partikel colloid yang cocok untuk menyebabkan tersebarnya partikel cahaya yang datang dengan sudut yang besar
2. Gerak Brown
Gerak Brown: gerak zig zag partikel yang diakibatkan benturan non-elastis antar partikel colloid dengan mediumnya. Gerak ini dapat digambarkan sesuai dengan sketsa atau gambar berikut ini:

Muatan Listrik
1. Adsorpsi
Adsorpsi : Koloid dapat bermuatan listrik karena adanya gaya Van der Waals terhadap ion atau molekul lain yang berada di sekitarnya. Misalnya seperti digambarkan berikut bagaimana sol $\mbox{As}_{2}\mbox{S}_{3}$ menjadi bermuatan negatif.

2. Elektroforesis
Elektroforesis: pergerakan partikel yang bermuatan menuju kutub listrik yang berlawanan (sesuai hukum Coulomb). Prosesnya dapat digambarkan sebagai berikut:

Kestabilan
Kestabilan koloid apabila rusak ditandai dengan terjadinya penggumpalan/koagulasi. Berikut ini cara yang dapat dilakukan untuk menjaga kestabilan colloid
1. Penambahan ion
Penambahan ion: setelah koloid menyerap ion akan terjadi gaya tolak-menolak dengan partikel sesamanya yang menyebabkan sistem lebih stabil dan tidak mudah menggumpal
2. Dialisis
Dialisis: proses mengeluarkan ion (yang mengganggu kestabilan) dengan cara memasukkan colloid ke dalam kantong yang terbuat dari selaput semipermeabel, kemudian dialiri cairan murni secara terus menerus, maka molekul ion tersebut akan menembus selaput dan terbawa keluar sehingga colloid menjadi stabil

3. Penambahan emulgator
Penambahan emulgator: suatu zat yang dapat menurunkan tegangan antar muka antara fase minyak dan air di dalam koloid sehingga mencegah terjadinya koagulasi akibat agregasi fase minyak yang terpisah dari fase air. Agregasi ini disebut pula misel/emulsi minyak dalam air yang digambarkan sebagai berikut.

Koagulasi
Koagulasi/penggumpalan dapat terjadi akibat beberapa hal berikut ini:
- Elektroforesis: proses ini menyebabkan partikel menjadi netral dan akhirnya menggumpal serta mengendap di sekitar elektroda
- Pemanasan: energi kinetik partikel akan meningkat, sehingga tumbukan menjadi lebih sering dan akhirnya mudah terjadi koagulasi
- Penambahan elektrolit dan pencampuran 2 koloid: apabila ke dalam colloid ditambahkan suatu elektrolit atau colloid lain yang bermuatan berlawanan, maka dapat terjadi koagulasi, misalnya colloid $\mbox{Fe(OH)}_{3}$ yang rusak kestabilannya bila ditambahkan elektrolit negatif, seperti $\mbox{PO}_{4}^{3-}$, akibat $\mbox{Fe}^{3+}$ yang keluar dan bereaksi dengan ion fosfat menghasilkan $\mbox{FePO}_{4}$
Pembuatan Koloid (Cooloid)
1. Dispersi
Dispersi: pemecahan gumpalan suspensi/partikel kasar menjadi lebih kecil sehingga tersebar dan berukuran sesuai partikel koloid
- Mekanik: menggerus/menggiling partikel kasar hingga berukuran colloid, contoh adalah pembuatan sulfur-urea, setelah penggilingan dicampur dengan air
- Peptisasi: menambahkan cairan ke dalam partikel kasar atau endapan sehingga pecah menjadi koloid. Contoh adalah pembuatan colloid $\mbox{Fe(OH)}_{3}$ dengan menambahkan $\mbox{FeCl}_{3}$ pada padatan $\mbox{Fe(OH)}_{3}$.
- Busur Bredig : mencelupkan logam yang akan dijadikan sebagai elektroda ke dalam air, kemudian diberi listrik tegangan tinggi sehingga atom-atom logam terlepas dari elektroda dan terlempar dalam air lalu mengalami pendinginan kembali sehingga terbentuk partikel colloid, seperti digambarkan dalam diagram berikut:

2. Kondensasi
Kondensasi: kebalikan dari dispersi, yaitu penggabungan partikel halus (partikel kecil) menjadi partikel yang lebih kasar sampai menjadi koloid
- Reaksi kimia, seperti reduksi (pembentukan koloid emas), oksidasi (pembentukan sol belerang dengan oksidasi hidrogen sulfida), hidrolisis $\mbox{(Al(OH)}_{3}$ atau metatesis/pertukaran ion.
- Pertukaran pelarut, contoh pembuatan colloid belerang dengan menambahkan air ke dalam larutan belerang dalam alkohol
S (aq) + alkohol + air $\rightarrow$ S (s) Larutan S sol belerang - Pendinginan berlebih, contoh pembuatan colloid es dengan mendinginkan campuran eter/kloroform dengan air.
- Dekomposisi rangkap, contoh: Pembuatan sol $\mbox{As}_{2}\mbox{S}_{3}$, dibuat dengan mengalirkan gas $\mbox{H}_{2}\mbox{S}$ dan asam arsenit $(\mbox{H}_{3}\mbox{AsO}_{3}$)
Contoh Soal dan Pembahasan
- Golongkan peristiwa berikut ini kepada sifat koloid yang sesuai
a. pembentukan delta sungai
b. proses cuci darah
c. penjernihan air dengan tawas
d. lampu menyinari kabut
e. penggumpalan lateks
f. analisis DNA
Pembahasan- koagulasi
- dialisis
- koagulasi
- efek Tyndall
- koagulasi
- elektroforesis
- Jelaskan sifat koloid yang menjadi dasar penggunaan alat Cottrel serta prinsip kerjanya!
Pembahasan
Alat Cottrel merupakan suatu mekanisme yang digunakan untuk menyaring gas buangan dari pabrik yang mengandung asap dan partikel berbahaya.
Prinsip kerjanya adalah sebagai berikut. Asap buangan pabrik dimasukkan ke dalam ruangan bertegangan listrik tinggi, sehingga elektron akan mengionkan molekul udara. Partikel asap akan menyerap ion positif dan tertarik ke elektroda negatif kemudian mengendap sehingga gas buangan ini keluar dalam bentuk padatan. Diagram alat Cottrel adalah sebagai berikut.




