Apa itu Golongan IIIA & IVA? Penasaran ingin mengetahuinya? Simak penjelasan lengkapnya di sini! Kami juga telah menyediakan soal atau kuis dengan tingkat kesulitan yang berbeda sebagai latihan.
Lewat pembahasan ini, kamu bisa belajar mengenai Golongan IIIA & IVA. kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Golongan 13 & 14 dalam bentuk pdf pada link dibawah ini:
Definisi
Unsur-unsur yang terletak pada kolom ke-13 dan 14 pada tabel periodik, meliputi :
- Golongan 13 : Boron, Aluminium, Galium, Indium, Thallium, Nihonium
- Golongan 14 : Karbon, Silikon, Germanium, Timah, Timbal, Flerovium
Karakteristik unsur golongan 13
- Memiliki tiga elektron valensi
- Kecuali Boron, semua anggotanya adalah logam.
- Semua anggotanya memiliki tingkat oksidasi +1 dan +3
- Meskipun sebagian besar bersifat logam, namun karena kepadatan muatan yang tinggi ia cenderung membentuk ikatan kovalen.
Karakteristik unsur golongan 14
- Memiliki empat elektron pada kulit terluar
- Kelogaman unsur golongan 14 berubah dari karbon (non logam) sampai timbal (logam), silikon dan germanium tergolong kedalam unsur semilogam
- Unsur karbon (kecuali senyawa karbid) dan silikon tidak membentuk senyawa ion
- Semakin kebawah pada golongan 14, atom semakin mudah melepaskan elektron.
Kekhasan Atom Karbon
- Karbon memiliki 4 elektron pada kulit terluar yang terdiri dari orbital 2s dan 2p (tidak ada 2d), sehingga karbon hanya dapat menggunakan empat orbital untuk berikatan.
- Unsur selain karbon dapat membentuk lebih banyak orbital karena memiliki orbital d seperti, misalnya silikon dapat membentuk senyawa $\mbox{SiF}_{6}^{2-}$
- Atom-atom karbon dapat membentuk rantia panjang atau bisa disebut dengan katenasi (catention), $\mbox{(-C-C-)}_{n}$
- Katenasi ini juga dapat terjadi pada unsur lain seperti Si-Si, Ge-Ge, Pb-Pb, namun ikatan yang terbentuk pada C-C lebih kuat dibandingkan dengan pada unsur lain (Energi ikat C-C paling besar).
- Atom karbon juga dapat membentuk ikatan rangkap (bisa 2 atau 3) baik dengan atom karbon maupun dengan atom lain seperti contoh berikut’
C-C ; C=C; $\mbox{C}\equiv\mbox{C}$
C=O; $\mbox{C}\equiv\mbox{N}$
Sifat Unsur
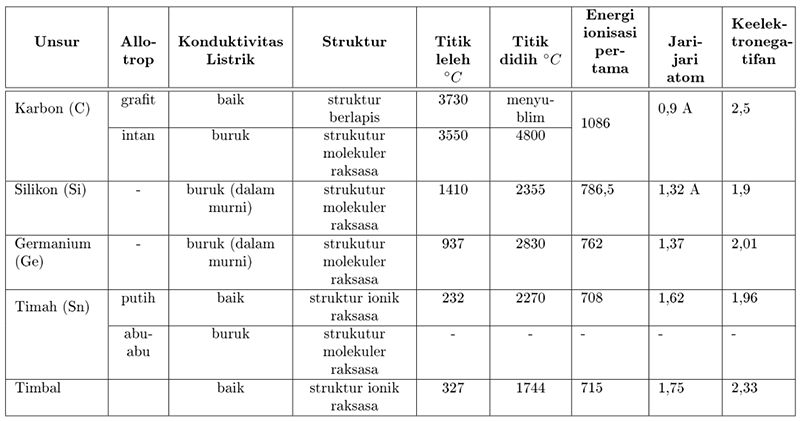
Kegunaan
- intan digunakan untuk bor, gerjaji, pemotong kaca, pemotong batuan
- silikon dan germanium banyak digunakan pada industri semikonduktor terutama komponen elektronik
- timah banyak digunakan untuk pelapisan baja untuk mencegah korosi, dan sebagai perekat komponen elektronik.
Oksida
Unsur golongan 14 dapat membentuk oksida dengan rumus XO dan $\mbox{XO}_{2}$. Timbal dapat membentuk $\mbox{Pb}_{3}\mbox{O}_{4}$

- oksidasi +4 semakin tidak stabil dari karbon sampai ke timbal
- $\mbox{Pb}^{4+}$ merupakan oksidator kuat
- Struktur $\mbox{SiO}_{2}$ adalah srtuktur molekuler raksasa (seperti pada intan)
- $\mbox{SiO}_{2}$ dan $\mbox{CO}_{2}$ adalah oksida asam
- $\mbox{GeO}_{2}$ , $\mbox{SnO}_{2}$ , $\mbox{PbO}$ merupakan oksida amfoter
- $\mbox{PbO}_{2}$ tidak dapat larut dalam asam nitrat, tetapi dapat larut dalam HCl pekat membentuk $\mbox{PbCl}_{4}$
- $\mbox{Pb}_{3}\mbox{O}_{4}$ adalah campuran dari PbO dan $\mbox{PbO}_{2}$
Contoh Soal dan Pembahasan
- Berikan perbedaan sifat antara karbon dalam alotropi intan dan grafit berkaitan dengan kemampuan penghantaran panas dan listrik!
Jawaban
Intan adalah suatu penghantar panas yang baik dan penghantar listrik yang buruk sementara sebaliknya grafit adalah penghantar panas yang buruk dan penghantar listrik yang baik.
