Selamat Datang dan Selamat Belajar di Wardaya College!
Di sini, kamu akan belajar tentang Elektrolisis melalui latihan soal interaktif dalam 3 tingkat kesulitan (mudah, sedang, sukar).
Apabila materi ini berguna, bagikan ke teman atau rekan kamu supaya mereka juga mendapatkan manfaatnya.
Latihan Soal Elektrolisis (Mudah)
Ringkasan kuis
0 dari 5 pertanyaan telah diselesaikan
Pertanyaan:
- 1
- 2
- 3
- 4
- 5
Informasi
You have already completed the quiz before. Hence you can not start it again.
Quiz is loading...
Anda harus masuk atau mendaftar untuk memulai kuis.
Anda harus menyelesaikan kuis dibawah ini, untuk memulai kuis ini:
Hasil
Hasil
0 dari 5 pertanyaan terjawab dengan benar
Waktu yang telah berlalu
Kategori
- Tidak Berkategori 0%
- 1
- 2
- 3
- 4
- 5
- Terjawab
- Tinjau
-
Pertanyaan ke 1 dari 5
1. Pertanyaan
Garam natrium sulfat dilarutkan dalam air . Ion apa saja yang terdapat dalam larutan?
BetulGaram natrium sulfat $(\mbox{Na}_{2}\mbox{SO}_{4})$ akan terionisasi dalam air menjadi:
$\mbox{Na}_{2}\mbox{SO}_{4}\rightarrow\mbox{Na}^{+}+\mbox{SO}_{4}^{2-}$ dan dalam air terdapat ion $\mbox{H}^{+}$ dan $\mbox{OH}^{-}$.
SalahGaram natrium sulfat $(\mbox{Na}_{2}\mbox{SO}_{4})$ akan terionisasi dalam air menjadi:
$\mbox{Na}_{2}\mbox{SO}_{4}\rightarrow\mbox{Na}^{+}+\mbox{SO}_{4}^{2-}$ dan dalam air terdapat ion $\mbox{H}^{+}$ dan $\mbox{OH}^{-}$.
-
Pertanyaan ke 2 dari 5
2. Pertanyaan
Salah satu cara ekstraksi logam Na adalah dengan elektrolisis lelehan oksidanya. Berikut ini pernyataan yang benar tentang elektrolisis lelehan $\mbox{Na}_{2}\mbox{O}$ dengan elektrode grafit adalah … kecuali.
BetulIon $\mbox{Na}^{+}$ akan bergerak ke elektrode negatif (katode).
SalahIon $\mbox{Na}^{+}$ akan bergerak ke elektrode negatif (katode).
-
Pertanyaan ke 3 dari 5
3. Pertanyaan
Reaksi yang terjadi di anoda pada elektrolisis larutan $\mbox{FeI}_{3}$ dengan elektrode inert adalah … .
BetulReaksi yang terjadi pada anoda adalah oksidasi, ion yang mengalami oksidasi adalah ion $\mbox{I}^{-}$.
$\mbox{2I}^{-}\rightarrow\mbox{I}_{2}+2e.$
SalahReaksi yang terjadi pada anoda adalah oksidasi, ion yang mengalami oksidasi adalah ion $\mbox{I}^{-}$.
$\mbox{2I}^{-}\rightarrow\mbox{I}_{2}+2e.$
-
Pertanyaan ke 4 dari 5
4. Pertanyaan
Pada proses elektrolisis seperti gambar berikut ini.

Reaksi yang terjadi pada elektrode A adalah … .
BetulElektrode A adalah anode (elektrode positif), yang dioksidasi adalah air karena ion sisa asam $\mbox{SO}_{4}^{2-}$tidak bisa dioksidasi.
$\mbox{2H}_{2}\mbox{O}\rightarrow4\mbox{H}^{+}\mbox{+O}_{2}+4e$
SalahElektrode A adalah anode (elektrode positif), yang dioksidasi adalah air karena ion sisa asam $\mbox{SO}_{4}^{2-}$tidak bisa dioksidasi.
$\mbox{2H}_{2}\mbox{O}\rightarrow4\mbox{H}^{+}\mbox{+O}_{2}+4e$
-
Pertanyaan ke 5 dari 5
5. Pertanyaan
Perhatikan proses elektrolisis berikut ini! X dan Y adalah elektrode inert.

Fenomena yang akan terjadi pada elektrode Y adalah … .
BetulElektrode Y adalah elektrode negatif, sehingga ion positif dari elektrolit $(\mbox{H}^{+})$ akan direduksi.
$\mbox{2H}^{+}+2e\rightarrow\mbox{H}_{2}$
SalahElektrode Y adalah elektrode negatif, sehingga ion positif dari elektrolit $(\mbox{H}^{+})$ akan direduksi.
$\mbox{2H}^{+}+2e\rightarrow\mbox{H}_{2}$
Latihan Soal Elektrolisis (Sedang)
Ringkasan kuis
0 dari 5 pertanyaan telah diselesaikan
Pertanyaan:
- 1
- 2
- 3
- 4
- 5
Informasi
You have already completed the quiz before. Hence you can not start it again.
Quiz is loading...
Anda harus masuk atau mendaftar untuk memulai kuis.
Anda harus menyelesaikan kuis dibawah ini, untuk memulai kuis ini:
Hasil
Hasil
0 dari 5 pertanyaan terjawab dengan benar
Waktu yang telah berlalu
Kategori
- Tidak Berkategori 0%
- 1
- 2
- 3
- 4
- 5
- Terjawab
- Tinjau
-
Pertanyaan ke 1 dari 5
1. Pertanyaan
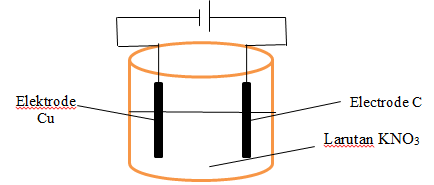
Pernyataan yang benar mengenai elektrolisis larutan $\mbox{KNO}_{3}$ berdasarkan gambar berikut adalah … .
 Betul
BetulPada anode terjadi reaksi oksidasi air menghasilkan gas $\mbox{O}_{2}$.
$\mbox{2H}_{2}\mbox{O}\rightarrow\mbox{4H}^{+}+\mbox{O}_{2}+4e$
SalahPada anode terjadi reaksi oksidasi air menghasilkan gas $\mbox{O}_{2}$.
$\mbox{2H}_{2}\mbox{O}\rightarrow\mbox{4H}^{+}+\mbox{O}_{2}+4e$
-
Pertanyaan ke 2 dari 5
2. Pertanyaan
Reaksi yang terjadi di katode pada elektrolisis larutan kalium iodida dengan elektrode tembaga adalah … .
BetulIon yang terdapat dalam larutan KI adalah: $\mbox{K}^{+}\mbox{H}^{+}\mbox{I}^{-}\mbox{OH}^{-}$
Spesi yang lebih mudah direduksi pada katoda (elektrode negatif) adalah $\mbox{2H}_{2}\mbox{O}+2e$$\rightarrow\mbox{2OH}^{-}+\mbox{H}_{2}.$
SalahIon yang terdapat dalam larutan KI adalah: $\mbox{K}^{+}\mbox{H}^{+}\mbox{I}^{-}\mbox{OH}^{-}$
Spesi yang lebih mudah direduksi pada katoda (elektrode negatif) adalah $\mbox{2H}_{2}\mbox{O}+2e$$\rightarrow\mbox{2OH}^{-}+\mbox{H}_{2}.$
-
Pertanyaan ke 3 dari 5
3. Pertanyaan
Pada suatu elektrolis reaksi yang terjadi di anoda dan katoda sebagai berikut:
- Anoda: $\mbox{Zn}\rightarrow\mbox{Zn}^{2+}+2e$
- Katode: $\mbox{Cu}^{2+}+2e\rightarrow\mbox{Cu}$
Komponen yang terdapat dalam proses elektrolisis di atas adalah … .
BetulLarutan $\mbox{CuCl}_{2}$ dengan elektrode Zn
Pada anode yang dioksidasi adalah Zn karena merupakan elektroda reaktif. Sehingga:
- Anode: $\mbox{Zn}\rightarrow\mbox{Zn}^{2+}+2e$
- Katode: $\mbox{Cu}^{2+}+2e\rightarrow\mbox{Cu}.$
SalahLarutan $\mbox{CuCl}_{2}$ dengan elektrode Zn
Pada anode yang dioksidasi adalah Zn karena merupakan elektroda reaktif. Sehingga:
- Anode: $\mbox{Zn}\rightarrow\mbox{Zn}^{2+}+2e$
- Katode: $\mbox{Cu}^{2+}+2e\rightarrow\mbox{Cu}.$
-
Pertanyaan ke 4 dari 5
4. Pertanyaan
Jika pada proses elektrolisis berikut ini digunakan elektrode inert, maka reaksi yang menghasilkan gas terdapat pada elektrode … .
 Betul
BetulElektrolisis larutan $\mbox{NiCl}_{2}$
- – Anoda (B) : $\mbox{2Cl}^{-}\rightarrow\mbox{Cl}_{2}+2e$
- – Katoda (A) : $\mbox{Ni}^{2+}+2e\rightarrow\mbox{Ni}$
Elektrolisis larutan asam sulfat- – Anode (D) : $\mbox{2H}_{2}\mbox{O}\rightarrow\mbox{4H}^{+}+\mbox{O}_{2}+4e$
- – Katoda (C) : $\mbox{2H}^{+}+2e\rightarrow\mbox{H}_{2}$
SalahElektrolisis larutan $\mbox{NiCl}_{2}$
- – Anoda (B) : $\mbox{2Cl}^{-}\rightarrow\mbox{Cl}_{2}+2e$
- – Katoda (A) : $\mbox{Ni}^{2+}+2e\rightarrow\mbox{Ni}$
Elektrolisis larutan asam sulfat- – Anode (D) : $\mbox{2H}_{2}\mbox{O}\rightarrow\mbox{4H}^{+}+\mbox{O}_{2}+4e$
- – Katoda (C) : $\mbox{2H}^{+}+2e\rightarrow\mbox{H}_{2}$
-
Pertanyaan ke 5 dari 5
5. Pertanyaan
Pada elektrolisis larutan di bawah ini yang menghasilkan gas hidrogen di anode adalah … .
Betul$\mbox{LiH}\rightarrow\mbox{Li}^{+}+\mbox{H}^{-}$
Katode : $\mbox{2H}_{2}\mbox{O}+2e$$\rightarrow\mbox{2OH}^{-}+\mbox{H}_{2}$
Anode: $\mbox{2H}^{-}\rightarrow\mbox{H}_{2}+2e.$
Salah$\mbox{LiH}\rightarrow\mbox{Li}^{+}+\mbox{H}^{-}$
Katode : $\mbox{2H}_{2}\mbox{O}+2e$$\rightarrow\mbox{2OH}^{-}+\mbox{H}_{2}$
Anode: $\mbox{2H}^{-}\rightarrow\mbox{H}_{2}+2e.$
Latihan Soal Elektrolisis (Sukar)
Ringkasan kuis
0 dari 5 pertanyaan telah diselesaikan
Pertanyaan:
- 1
- 2
- 3
- 4
- 5
Informasi
You have already completed the quiz before. Hence you can not start it again.
Quiz is loading...
Anda harus masuk atau mendaftar untuk memulai kuis.
Anda harus menyelesaikan kuis dibawah ini, untuk memulai kuis ini:
Hasil
Hasil
0 dari 5 pertanyaan terjawab dengan benar
Waktu yang telah berlalu
Kategori
- Tidak Berkategori 0%
- 1
- 2
- 3
- 4
- 5
- Terjawab
- Tinjau
-
Pertanyaan ke 1 dari 5
1. Pertanyaan
Pernyataan yang benar mengenai sel elektrolisis berikut adalah … .
 Betul
BetulReaksi oksidasi di anode: $\mbox{2O}^{2-}\rightarrow\mbox{O}_{2}+4e$, selanjutnya gas oksigen bereaksi dengan C (elektrode) menghasilkan gas $\mbox{CO}_{2}$.
SalahReaksi oksidasi di anode: $\mbox{2O}^{2-}\rightarrow\mbox{O}_{2}+4e$, selanjutnya gas oksigen bereaksi dengan C (elektrode) menghasilkan gas $\mbox{CO}_{2}$.
-
Pertanyaan ke 2 dari 5
2. Pertanyaan
Pada sel elektrolisis berikut, pada sel manakah terdapat jumlah ion paling banyak di dalam larutannya setelah elektrolisis selesai?
 Betul
BetulPada sel 1 terjadi reaksi:
- Anode: $\mbox{Cu}\rightarrow\mbox{Cu}^{2+}+2e$
- Katode: $\mbox{2H}^{+}+2e\rightarrow\mbox{H}_{2}$
Pada sel 2 terjadi reaksi:- Anode: $\mbox{2O}^{2-}\rightarrow\mbox{O}_{2}+4e$
- Katode: $\mbox{K}^{+}+e\rightarrow\mbox{K}$
Maka pada sel 1 lah terdapat paling banyak ion di dalam larutan setelah proses elektrolisis berlangsung.SalahPada sel 1 terjadi reaksi:
- Anode: $\mbox{Cu}\rightarrow\mbox{Cu}^{2+}+2e$
- Katode: $\mbox{2H}^{+}+2e\rightarrow\mbox{H}_{2}$
Pada sel 2 terjadi reaksi:- Anode: $\mbox{2O}^{2-}\rightarrow\mbox{O}_{2}+4e$
- Katode: $\mbox{K}^{+}+e\rightarrow\mbox{K}$
Maka pada sel 1 lah terdapat paling banyak ion di dalam larutan setelah proses elektrolisis berlangsung. -
Pertanyaan ke 3 dari 5
3. Pertanyaan
Pada proses elektrolisis berikut, gas oksigen dihasilkan pada elektrode W dan logam aluminium pada X.

Berikan label yang tepat pada proses di atas.
BetulElektrolisis logam yang reaktif (mempunyai potensial reduksi negatif) harus dalam kondisi lelehan oksidanya untuk mendapatkan hasil logam tersebut. Sehingga,
$\mbox{Al}_{2}\mbox{O}_{3}(\ell)\rightarrow\mbox{2Al}^{3+}+3\mbox{O}^{2-}$
Anode : $\mbox{2O}^{2-}\rightarrow\mbox{O}_{2}+4e$
Katode : $\mbox{Al}^{3+}+3e\rightarrow\mbox{Al}.$
SalahElektrolisis logam yang reaktif (mempunyai potensial reduksi negatif) harus dalam kondisi lelehan oksidanya untuk mendapatkan hasil logam tersebut. Sehingga,
$\mbox{Al}_{2}\mbox{O}_{3}(\ell)\rightarrow\mbox{2Al}^{3+}+3\mbox{O}^{2-}$
Anode : $\mbox{2O}^{2-}\rightarrow\mbox{O}_{2}+4e$
Katode : $\mbox{Al}^{3+}+3e\rightarrow\mbox{Al}.$
-
Pertanyaan ke 4 dari 5
4. Pertanyaan
Bila pada sel elektrolisis berikut gas oksigen dihasilkan pada elektrode W dan logam aluminium pada X digunakan suatu sampel sebanyak 5 gram dengan kemurnian 82%, berapakah volume gas maksimal (STP) yang dapat diukur setelah proses berlangsung?
Betul$\begin{aligned}\mbox{Massa sampel} & =\mbox{massa Al}_{2}\mbox{O}_{3}\\
& =\frac{82}{100}\times5\mbox{ gr}\\
& =4,1\mbox{ gr}
\end{aligned}
$Setarakan reaksi-reaksi termasuk redoks yang terjadi:
$\mbox{Al}_{2}\mbox{O}_{3}(\ell)$$\rightarrow\mbox{2Al}^{3+}+3\mbox{O}^{2-}$
$\mbox{6O}^{2-}\rightarrow\mbox{3O}_{2}+12e$
$\mbox{4Al}^{3+}+12e\rightarrow\mbox{4Al}$
Maka mol gas oksigen yang terbentuk adalah 3/2 dari mol alumunium oksida. Sehingga didapatkan:
$\begin{aligned}\mbox{Volume oksigen} & =22,4\mbox{L/mol}\times\frac{3}{2}\times\frac{4,1\mbox{ gr}}{102\mbox{ gr/mol}}\\
& =1,344\mbox{ L}.
\end{aligned}
$Salah$\begin{aligned}\mbox{Massa sampel} & =\mbox{massa Al}_{2}\mbox{O}_{3}\\
& =\frac{82}{100}\times5\mbox{ gr}\\
& =4,1\mbox{ gr}
\end{aligned}
$Setarakan reaksi-reaksi termasuk redoks yang terjadi:
$\mbox{Al}_{2}\mbox{O}_{3}(\ell)$$\rightarrow\mbox{2Al}^{3+}+3\mbox{O}^{2-}$
$\mbox{6O}^{2-}\rightarrow\mbox{3O}_{2}+12e$
$\mbox{4Al}^{3+}+12e\rightarrow\mbox{4Al}$
Maka mol gas oksigen yang terbentuk adalah 3/2 dari mol alumunium oksida. Sehingga didapatkan:
$\begin{aligned}\mbox{Volume oksigen} & =22,4\mbox{L/mol}\times\frac{3}{2}\times\frac{4,1\mbox{ gr}}{102\mbox{ gr/mol}}\\
& =1,344\mbox{ L}.
\end{aligned}
$ -
Pertanyaan ke 5 dari 5
5. Pertanyaan
Bila diketahui data berikut:
- $\mbox{Cu}^{2+}+2e\rightleftharpoons\mbox{Cu}$ $E^{\circ}\mbox{=+0,337 V}$
- $2\mbox{H}_{2}\mbox{O}+2e\rightleftharpoons\mbox{H}_{2}+2\mbox{OH}^{-}$ $E^{\circ}\mbox{=-0,8277 V}$
- $2\mbox{H}_{2}\mbox{O}\rightleftharpoons\mbox{O}_{2}+4\mbox{H}^{+}+4e$ $E^{\circ}\mbox{=-1,229 V}$
- $\mbox{Cl}_{2}+2e\rightleftharpoons2\mbox{Cl}^{-}$ $E^{\circ}\mbox{=+1,36 V}$
Berapakah besar energi bebas Gibbs dari elektrolisis yang dilakukan pada sel 1 sesuai diagram berikut (konstanta faraday= 96500) ?BetulPotensial sel pada reaksi ini adalah:
$\begin{aligned}E^{\circ}\mbox{katode-}E^{\circ}\mbox{anode} & =+0,337-0\mbox{V}\\
& \mbox{=0,337 V}.
\end{aligned}
$Maka,
$\begin{aligned}\Delta G^{\circ} & =-nFE^{\circ}\mbox{sel}\\
& =-2\times96485\times0,337\mbox{ J}\\
& =-65401\mbox{ J}.
\end{aligned}
$SalahPotensial sel pada reaksi ini adalah:
$\begin{aligned}E^{\circ}\mbox{katode-}E^{\circ}\mbox{anode} & =+0,337-0\mbox{V}\\
& \mbox{=0,337 V}.
\end{aligned}
$Maka,
$\begin{aligned}\Delta G^{\circ} & =-nFE^{\circ}\mbox{sel}\\
& =-2\times96485\times0,337\mbox{ J}\\
& =-65401\mbox{ J}.
\end{aligned}
$