Kalau kamu ingin belajar Senyawa Oksida secara lebih mendalam, coba simak penjelasan yang ada di sini. Setelah menerima materi, kamu bisa langsung mempraktikkannya dengan mengerjakan latihan soal yang telah kami sediakan.
Lewat pembahasan ini, kamu bisa belajar mengenai Senyawa Oksida. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Senyawa Oksida dalam bentuk pdf pada link dibawah ini:
Jenis-jenis Oksida
Pada pemelajaran senyawa oksida ini kita akan belajar mengenai; senyawa oksida asam, oksida amfoter, dan juga reaksi oksida basa dengan asam, untuk lebih jelasnya berikut akan diulans lengkap mengenai jenis-jenis Oksida.
1. Oksida Asam
Oksida asam: umumnya dibentuk unsur non logam yang berikatan dengan oksigen. Ciri-cirinya:
- Larut dalam air membentuk larutan asam
- Oksida asam bereaki dengan basa membentuk garam dan air
$\mbox{CO}_{2}(g)+\mbox{H}_{2}\mbox{O}(l)\rightarrow\mbox{H}_{2}\mbox{CO}_{3}(aq)$ - Oksida asam bereaki dengan basa membentuk garam dan air
$\mbox{CO}_{2}(g)+\mbox{NaOH}(aq)\rightarrow\mbox{Na}_{2}\mbox{CO}_{3}(aq)+\mbox{H}_{2}\mbox{O}(l)$ - Contoh oksida asam lainnya adalah $\mbox{SO}_{2}$,
$\mbox{SO}_{3}$, $\mbox{P}_{4}\mbox{O}_{10}$ - Oksida asam tidak bereaksi dengan asam
Jadi kalau ada pertanyaan sebutkan ciri-ciri senyawa oksida asam 5 ciri-ciri diatas adalah jawabannya.
2. Oksida Basa
Oksida Basa: umumnya dibentuk unsur logam + oksigen
- Wujud padat (RTP)
- Sebagian besar oksida basa tidak larut dalam air
- Beberapa oksida basa seperti $\mbox{Na}_{2}\mbox{O}$ , $\mbox{K}_{2}\mbox{O}$ dan $\mbox{CaO}$ dapat larut dan membentuk larutan basa
$\mbox{CaO}(s)+\mbox{H}_{2}\mbox{O}(l)\rightarrow\mbox{Ca(OH)}_{2}(aq)$ - Oksida basa dapat bereaksi dengan asam membentuk garam dan air
$\mbox{CaO}(s)+2\mbox{HCl}(aq)\rightarrow\mbox{CaCl}_{2}(aq)+\mbox{H}_{2}\mbox{O}(l)$
Dari uraian diatas kamu juga bisa membuat tabel oksida basa untuk memudahkanmu dalam belajar.
3. Oksida Amfoter
Oksida Amfoter : oksida yang dapat bereaksi dengan asam maupun basa, biasanya terbentuk dari unsur logam, contoh ZnO, PbO, aluminium.
- $\mbox{ZnO}(s)+2\mbox{HCl}(aq)\rightarrow\mbox{ZnCl}_{2}(aq)+\mbox{H}_{2}\mbox{O}(l)$
asam - $\mbox{ZnO}(s)+2\mbox{NaOH}(aq)\rightarrow\mbox{Na}_{2}\mbox{ZnO}_{2}(aq)+\mbox{H}_{2}\mbox{O}(l)$
basa
- Oksida Netral: oksida dari non logam yang tidak bereaksi dengan asam maupun basa, serta sukar larut dalam air, contoh: $\mbox{H}_{2}\mbox{O},\mbox{ CO, NO}$
Kegunaan Oksida
Suatu oksida terutama berperan sebagai bijih (ore) yang akan diekstraksi untuk menghasilkan logam murninya, sebagai contoh aluminium oksida, besi (III) oksida dan lainnya. Ekstraksi ini dapat dilakukan melalui proses reduksi sebagai berikut:
- Reduksi dengan karbon: digunakan dalam produksi besi dari oksidanya
- Reduksi dengan pemanasan : digunakan untuk logam dengan reaktivitas yang rendah, seperti perak
- Reduksi dengan reaksi pendesakan logam : logam yang lebih reaktif mampu mendesak metal yang lebih rendah reaktivitasnya dari senyawa oksidanya
- Reduksi dengan hidrogen : hidrogen dapat mendesak oksida dari logam yang rendah reaktivitasnya menghasilkan air
- Reduksi dengan elektrolisis : digunakan untuk logam-logam dengan reaktivitas tinggi.
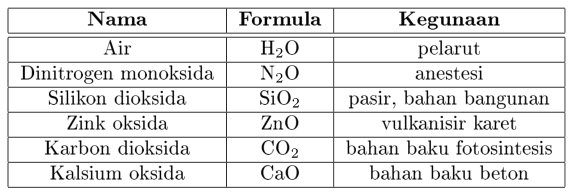
Selain digunakan sebagai sumber logam, berikut beberapa oksida yang umum dan penggunaannya oleh manusia:
Contoh Soal dan Pembahasan
- Berdasarkan sifat oksidanya, tentukan tren keasaman pada unsur-unsur berikut: Mg, Na, Al, Si , S, P.
Jawaban
Seperti kita ketahui, oksida unsur logam (terletak di sebelah kiri tabel periodik) akan membentuk oksida basa sementara oksida non logam (terletak sebelah kanan) membentuk asam.
Sehingga dalam satu periode, dari kiri ke kanan kecenderungan oksida suatu unsur akan semakin asam, sehingga urutan keasamannya adalah: Na, Mg, Al, Si, P, S. - Bila 0,3 mol oksida fosfat, $\mbox{P}_{4}\mbox{O}_{10}$ dilarutkan dalam 200 mL air, tentukan konsentrasi larutan yang terbentuk serta kira-kira rentang pH nya bila $K_{a}$ larutan yang terbentuk adalah $7,1\times10^{-3}$! (asumsikan larut sempurna)
Jawaban
Reaksi yang terjadi :
$\mbox{P}_{4}\mbox{O}_{10}+6\mbox{H}_{2}\mbox{O}\rightarrow4\mbox{H}_{3}\mbox{PO}_{4}$
Maka, mol asam fosfat yang terbentuk:
$\frac{4\mbox{ mol}\mbox{H}_{3}\mbox{PO}_{4}}{1\mbox{ mol}\mbox{P}_{4}\mbox{O}_{10}}\times0,3\mbox{ mol}\mbox{ P}_{4}\mbox{O}_{10}=1,2\mbox{ mol }\mbox{H}_{3}\mbox{PO}_{4}$
Maka,
$\begin{aligned}\mbox{H}_{3}\mbox{O}^{+} & =\sqrt{K_{a}[\mbox{H}_{3}\mbox{PO}_{4}]}\\
& =\sqrt{7,1\times10^{-3}\times6}\\
& =\sqrt{426\times10^{-4}}\\
& =0,2064\\
pH & =-\log0,2064\\
& =0,6853
\end{aligned}$


