Masih sering bingung dengan Hukum Laju Reaksi? Yuk, simak penjelasan lengkapnya lewat uraian berikut. Setelahnya, kamu juga bisa mengerjakan latihan soal yang telah disediakan untuk mengasah kemampuan belajarmu.
Lewat pembahasan ini, kamu bisa belajar mengenai Hukum Laju Reaksi. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Hukum Laju Reaksi dalam bentuk pdf pada link dibawah ini:
Definisi
Hubungan kuantitatif antara konsentrasi pereaksi dengan laju reaksi.
Persamaan Laju Reaksi
Bila diketahui suatu reaksi:
$l\mbox{A}+m\mbox{B}\rightarrow n\mbox{C}+o\mbox{D}$
Maka persamaan lajunya dapat dinyatakan sebagai
$v=k[A]^{x}[B]^{y}$
dimana,
$k=$ tetapan jenis reaksi
$x=$ orde (tingkat atau pangkat) reaksi terhadap pereaksi A
$y=$ orde (tingkat atau pangkat) reaksi terhadap pereaksi B
Seperti terlihat, tidak ada hubungan antara koefisien stoikiometri reaksi dengan orde masing-masing pereaksi, dimana orde ini hanya dapat ditentukan melalui eksperimen.
Tetapan jenis reaksi adalah suatu konstanta atau tetapan yang harganya bergantung pada jenis pereaksi, suhu dan katalis. Setiap reaksi mempunyai harga $k$ tertentu pada suhu tertentu, harganya akan berubah bila suhu diubah.
Nilai $k$ berbanding lurus dengan laju reaksi, semakin besar nilainya maka semakin cepat reaksi tersebut berjalan. Kenaikan suhu dan penggunaan katalis umumnya memperbesar nilai $k$.
Menentukan Persamaan Laju Reaksi
Persamaan laju suatu reaksi tidak memiliki hubungan dengan stoikiometri reaksi, tetapi ditentukan melalui percobaan, salah satu metode yang sering digunakan adalah metode laju awal.
Menurut cara ini, laju diukur pada awal reaksi dengan konsentrasi yang berbeda-beda. Sebagai contoh pada reaksi antara HCl dan natrium karbonat berikut:
$2\mbox{HCl}+\mbox{Na}_{2}\mbox{CO}_{3}\rightarrow2\mbox{NaCl}+\mbox{CO}_{2}+\mbox{H}_{2}\mbox{O}$
didapat data berikut:

persamaan laju dapat ditulis sebagai berikut:
$v=k[\mbox{HCl]}^{x}[\mbox{Na}_{2}\mbox{CO}_{3}]^{y}$
dimana $x\mbox{ dan }y$ dari rumus persamaan laju reaksi yang benar adalah orde reaksi masing-masing pereaksi, untuk menentukannya kita bandingkan data percobaan dimana salah satu pereaksi dibuat sebagai variabel kontrol (nilainya tidak berubah).
Pada data di atas kita lihat diantara percobaan 1 dan 4 nilai konsentrasi $\mbox{Na}_{2}\mbox{CO}_{3}$ tidak berubah, maka orde reaksi terhadap HCl dapat kita tentukan:
$\begin{aligned}\frac{v_{1}}{v_{4}} & =\frac{k[\mbox{HCl]}_{1}^{x}[\mbox{Na}_{2}\mbox{CO}_{3}]_{1}^{y}}{k[\mbox{HCl]}_{4}^{x}[\mbox{Na}_{2}\mbox{CO}_{3}]_{4}^{y}}\\
\frac{5,4}{10,8} & =\frac{0,01^{x}\times0,2^{y}}{0,02^{x}\times0,2^{y}}\\
\frac{1}{2} & =\left(\frac{1}{2}\right)^{x}\\
x & =1
\end{aligned}
$
Orde terhadap HCl adalah satu. Sementara itu data percobaan 2 dan 3 dapat kita gunakan untuk mengetahui orde terhadap $\mbox{Na}_{2}\mbox{CO}_{3}$:
$\begin{aligned}\frac{v_{2}}{v_{3}} & =\frac{k[\mbox{HCl]}_{2}^{x}[\mbox{Na}_{2}\mbox{CO}_{3}]_{2}^{y}}{k[\mbox{HCl]}_{3}^{x}[\mbox{Na}_{2}\mbox{CO}_{3}]_{3}^{y}}\\
\frac{10,9}{21,8} & =\frac{0,2^{x}\times0,202^{y}}{0,2^{x}\times0,404^{y}}\\
\frac{1}{2} & =\left(\frac{1}{2}\right)^{y}\\
y & =1
\end{aligned}
$
Orde terhadap $\mbox{Na}_{2}\mbox{CO}_{3}$ adalah satu. Sehingga persamaan laju keseluruhan adalah
$v=k[\mbox{HCl}][\mbox{Na}_{2}\mbox{CO}_{3}]$
Contoh Soal Persamaan Laju Reaksi Beserta Jawabannya
- Diketahui reaksi $2\mbox{NO}+\mbox{H}_{2}\rightarrow\mbox{N}_{2}\mbox{O}+\mbox{H}_{2}\mbox{O}$. Bila diketahui orde reaksi terhadap NO adalah 1 sementara terhadap $\mbox{H}_{2}$ adalah 0, tuliskan persamaan laju untuk reaksi ini!
Jawaban
$v=k[\mbox{NO}]^{1}[\mbox{H}_{2}]^{0}$
$v=k[\mbox{NO}]$
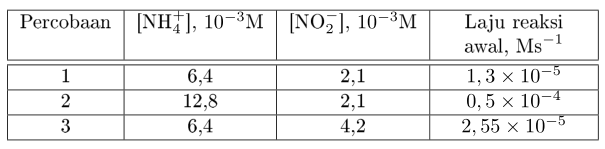
– - Diketahui data berikut untuk reaksi ion amonium dan nitrit berikut:

Tentukan persamaan laju reaksinya!
–
Jawaban
Bandingkan percobaan 1 dan 3 :$\begin{aligned}\frac{v_{1}}{v_{3}} & =\frac{[\mbox{NH}_{4}^{+}]_{1}^{x}[\mbox{NO}_{2}^{-}]_{1}^{y}}{[\mbox{NH}_{4}^{+}]_{3}^{x}[\mbox{NO}_{2}^{-}]_{3}^{y}}\\
\frac{1,3\times10^{-5}}{2,55\times10^{-5}} & =\left(\frac{2,1}{4,2}\right)^{y}\\
y & =1
\end{aligned}
$
–
Bandingkan percobaan 1 dan 2
–
$\begin{aligned}\frac{v_{1}}{v_{2}} & =\frac{[\mbox{NH}_{4}^{+}]_{1}^{x}[\mbox{NO}_{2}^{-}]_{1}^{y}}{[\mbox{NH}_{4}^{+}]_{2}^{x}[\mbox{NO}_{2}^{-}]_{2}^{y}}\\
\frac{1,3\times10^{-5}}{5\times10^{-4}} & =\left(\frac{6,4}{12,8}\right)^{x}\\
x & =2
\end{aligned}
$
–
Sehingga persamaan laju keseluruhan $v=k[\mbox{NH}_{4}^{+}]^{2}[\mbox{NO}_{2}^{-}]$