Apakah kamu sedang mencari pembahasan mengenai Benzena? Di sini, kami memiliki uraian lengkap tentang pembahasan tersebut. Tak lupa, telah tersedia pula latihan soal yang bisa coba kamu kerjakan.
Lewat pembahasan ini, kamu bisa belajar mengenai Benzena. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Benzena dalam bentuk pdf pada link dibawah ini:
Definisi
Pengertian Benzena (dalam bahasa Inggris Benzene) adalah senyawa kimia organik yang merupakan cairan tak berwarna dan mudah terbakar serta mempunyai bau yang manis. Benzena juga dikenal dengan rumus kimia C6H6, PhH, dan benzol.
1. Struktur benzena : pengaturan unsur-unsur yang terdapat pada benzene, suatu senyawa dengan 6 karbon berbentuk cincin dengan ikatan rangkap terkonjugasi dan terdelokalisasi.
2. Karakteristik benzena, meliputi sifat fisis, kimia dan sifatnya sebagai senyawa aromatis.
3. Pembuatan benzena : Proses dan cara membuat atau mensintesis benzene.
4. Hidrokarbon aromatik : Senyawa hidrokarbon yang memenuhi persyaratan aromatik Huckel, meliputi cincin siklis, planar dan jumlah elektron $\pi$ nya $4n+2$, $n=$ bilangan bulat.
Struktur Benzena
Senyawa benzene pertama kali ditemukan oleh Michael Faraday dari suatu gas yang digunakan untuk lampu penerangan. Sejak penemuannya banyak teori yang berkembang mengenai struktur molekul benzene. Pada 1865, August Kekule mengemukakan teorinya yang masih diterima hingga sekarang, dimana menurutnya senyawa benzene berbentuk siklik (rantai tertutup) dan segi enam beraturan (heksagonal) dengan sudut antar atom $120^{\circ}$.
Dalam ikatan antar atom C terdapat tiga buah ikatan rangkap dua yang berselang-seling dengan ikatan tunggal, inilah yang disebut ikatan rangkap terkonjugasi. Struktur ini dapat digambarkan berupa cincin segi enam, dimana tiap sudut adalah atom C dan atom H tidak digambarkan, sebagai berikut:

Tanda panah bolak-balik menunjukkan struktur tersebut adalah struktur resonansi. Resonansi adalah perubahan posisi elektron pada atom-atom dalam senyawa, sehingga tidak ada satu struktur yang benar-benar pasti untuk menggambarkan senyawa tersebut, dalam hal ini karena ikatan rangkap yang terdelokalisasi atau berpindah-pindah
Delokalisasi ini terjadi akibat orbital p bebas pada setiap atom C. Orbital yang saling bertindihan (overlap) sisi membentuk cincin awan elektron yang mengapit cincin benzena di atas dan bawah cincinnya seperti gambar berikut.

Setiap atom C benzena memiliki sifat dan fungsi yang sama, hal ini dapat diketahui dari panjang ikatan antar atom C, semuanya berkisar 140 pm, yang terhitung lebih panjang dari ikatan rangkap C=C biasa (133 pm) dan lebih pendek dari ikatan tunggal C-C (154 pm).
Sifat Benzena
Benzena memiliki sifat-sifat sebagai berikut:
1. Sifat fisik : zat cair yang volatil (mudah menguap) dan tidak berwarna.
Titik didih benzena dan turunannya bervariasi dari $80-250^{\circ}$C. Sementara titik lelehnya bervariasi, paling tinggi adalah $122^{\circ}$C yang dimiliki salah satu turunan benzene, yakni asam benzoat.
Variasi titik didih dan titik leleh ini disebabkan pengaruh gugus fungsi atau substituen benzene, hal ini juga menyebabkan kelarutannya di dalam air bervariasi, asam benzoat, fenol dan anilin relatif mudah larut di dalam air karena kemampuannya membentuk ikatan hidrogen. Sebaliknya benzene dan turunannya yang non polar sukar larut di air.
2. Sifat kimia : bersifat toksik, tidak reaktif , namun mudah terbakar.
Benzena hanya reaktif terhadap reaksi substitusi. Dari penemuannya pertama kali, benzena dan turunannya disebut sebagai senyawa aromatik karena ia memiliki aroma yang khas. Seiring berjalannya waktu, ditemukan senyawa-senyawa turunan benzene yang tidak berbau, hal ini menyebabkan makna aromatis meluas.
Kriteria untuk suatu senyawa aromatis
Berikut ini kriteria untuk suatu senyawa aromatis:
- Senyawa harus memiliki struktur cincin dengan orbital p yang bertumpang-tindih (overlap)
- Jumlah elektron pi memenuhi 4n+2, n adalah bilangan bulat.
Senyawa yang tidak memenuhi syarat pertama disebut senyawa non-aromatik, senyawa yang memenuhi aturan pertama namun hanya memiliki jumlah elektron pi sebesar 4n disebut antiaromatik.
Persyaratan senyawa aromatik di atas disebut juga aturan Huckel, dan berlaku untuk semua molekul, bahkan ion sekalipun, sebagai contoh, tentukan apakah senyawa di bawah ini bersifat aromatik?
![]()
Pembuatan Benzena
Benzena dan turunannya dapat ditemui dengan mudah dalam kehidupan sehari-hari, mulai dari asap rokok hingga aroma buah ceri dan almond, selain itu telah banyak ditemukan kegunaannya, oleh sebab itu kita perhatikan cara-cara pembuatan benzene berikut:
1. Polimerisasi 3 molekul asetilena dengan mengalirkannya melalui kaca berpijar:

2. Reaksi antara kalsium benzoat dengan kalsium hidroksida serta suhu tinggi:
$\mbox{Ca}\left(\mbox{C}_{6}\mbox{H}_{5}\mbox{COO}\right)_{2}+\mbox{Ca}\left(\mbox{OH}\right)_{2}\rightarrow2\mbox{C}_{6}\mbox{H}_{6}+2\mbox{CaCO}_{3}$
4. Proses reforming atau penataan ulang nafta pada industri petroleum, dimana fraksi ini dicampurkan dengan gas hidrogen kemudian diekspos dengan katalis berbasis platinum atau rhenium, suhu $500-525^{\circ}$C tekanan 8-50 atm.
5. Reaksi hidrodealkilasi toluen. Pada proses ini, toluen (metilbenzena) dicampur dengan gas hidrogen, dilewatkan pada katalis berbasis krom, molibdenum atau platinum oksida pada $500-600^{\circ}$C dan tekanan 40-60 atm.
Hidrokarbon Aromatik (Materi Olimpiade Kimia)
Pada awalnya, dinamakan demikian karena didapati senyawa aromatis, seperti benzena, memiliki aroma/bau yang khas. Namun seiring berjalannya waktu ditemukan banyak senyawa-senyawa turunan benzene yang tidak berbau. Meski demikian, istilah “aromatis” tetap digunakan untuk mempermudah penggolongan senyawa-senyawa kelompok benzena.
1. Nomenklatur Benzena dan Turunannya
Berikut ini senyawa-senyawa benzena monosubstitusi yang umum:
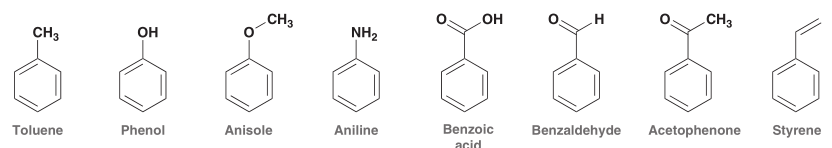
Apabila substituen benzene memiliki rantai karbon yang lebih panjang maka cincin benzena dianggap sebagai gugus fungsi dengan nama fenil, yang sering dilambangkan dengan Ph atau huruf Yunani phi ($\phi$)
Untuk senyawa benzena dengan 2 atau lebih substituen, maka ikuti langkah berikut:
1. Identifikasi substituen prioritas dan tetapkan sebagai rantai utama (dapat menggunakan nama umum benzene monosubstitusinya)
2. Identifikasi substituen lainnya, berikan nomor dan susun secara alfabet seperti biasanya, atau bila dimungkinkan gunakan orto (posisi 1,2); meta (posisi 1,3) atau para (posisi 1,4)
Contoh pemberian nomor dan nama yang tepat:

Sehingga nama senyawa di atas: 5-bromo-2-klorofenol
2. Aromatisitas
Suatu senyawa aromatis harus memenuhi syarat-syarat di bawah ini, yang sering disebut aturan Huckel:
1. Memiliki sistem ikatan $\pi$ terkonjugasi
2. Memiliki geometri molekul planar
3. Memiliki bentuk molekul siklik
4. Memiliki elektron $\pi$ sejumlah 4n+2, dimana n adalah bilangan bulat dari 0, 1, 2 dst.
3. Reaksi Substitusi Benzena
Rangkuman reaksi-reaksi penting benzena adalah sebagai berikut:

Mekanisme umum untuk reaksi substitusi aromatik elektrofilik:
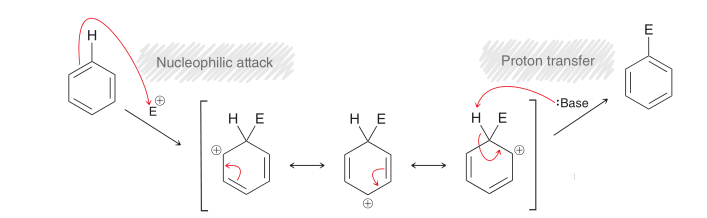
Yang harus diperhatikan adalah proses pembentukan gugus elektrofilik, terutama kasus khusus untuk reaksi nitrasi, pembentukan ion nitronium berjalan sebagai berikut

4. Gugus Pengaktivasi Cincin Benzena
Karakter khususnya adalah suatu gugus pendorong elektron atau atom yang terikat ke benzene memiliki pasangan elektron bebas. Semua gugus pengaktivasi adalah penunjuk orto-para, yang disebabkan karena delokalisasi pasangan elektron bebas gugusnya sebagai berikut

Karena muatan negatif terletak pada posisi ortho dan para maka substituen elektrofil pun lebih mudah masuk pada posisi itu.
5. Gugus Pendeaktivasi Cincin Benzena
Sebaliknya, suatu gugus pendeaktivasi akan menarik elektron dari cincin benzene dan membentuk resonansi berikut:

Karena pada posisi ortho dan para bermuatan positif, menyebabkan elektrofil yang masuk akan sulit berada pada posisi tersebut dan akan masuk ke posisi meta. Oleh sebab itu sebagian besar gugus pendeaktivasi adalah pengarah meta, kecuali gugus halogen.
Suatu halogen memiliki PEB yang dapat membentuk resonansi seperti milik gugus pengaktivasi, meski demikian ia juga memiliki efek penarik elektron yang cukup kuat sehingga termasuk gugus pendeaktivasi.
Sehingga dapat disimpulkan sebagai berikut untuk pengaruh gugus pertama terhadap substitusi kedua:

Contoh Soal dan Pembahasan
1. Jenis reaksi organik apakah (diantara adisi, eliminasi, substitusi, oksidasi) yang paling mudah dilakukan kepada benzena?
Jawaban
Suatu benzena paling mudah disubstitusi dibandingkan diadisi, dieliminasi atau dioksidasi, karena reaksi substitusi tidak mengubah susunan cincin benzene yang sudah sangat stabil.
2. Histamin yang berperan untuk meredakan reaksi alergi memiliki struktur seperti di bawah ini. Tentukan apakah ia bersifat aromatik, nonaromatik atau anti aromatik?

Jawaban
Kita perlu memperhitungkan apakah ada PEB milik atom N yang terlibat pada overlap orbital p. Bila kita tuliskan semua elektron yang mungkin terlibat pada overlap:

PEB milik N kiri bawah tidak terlibat dalam overlap, karena tidak terkonjugasi dengan ikatan rangkap lainnya (harus berjarak 1 ikatan tunggal).
Sehingga total terdapat 6 elektron pi, yang memenuhi aturan Huckel, sehingga senyawa histamin bersifat aromatik.
3. Tuliskan reaksi lengkap untuk reaksi hidrodealkilasi toluena!
Jawaban
Dari nama proses yang berlangsung, kita analisis:
hidro + dealkilasi + toluen
(a) hidro: melibatkan gas hidrogen
(b) dealkilasi : pemutusan alkil dari cincin benzena
Alkil yang terputus adalah $-\mbox{CH}_{3}$, dari satu mol gas hidrogen $\left(\mbox{H}_{2}\right)$ satu atom H akan masuk ke cincin benzene menggantikan alkil, 1 atom H lainnya akan masuk ke alkil $-\mbox{CH}_{3}$ agar stabil sebagai senyawa metana $\left(\mbox{CH}_{4}\right)$.
Sehingga secara keseluruhan reaksinya adalah:
$\mbox{C}_{6}\mbox{H}_{5}\mbox{CH}_{3}+\mbox{H}_{2}\rightarrow\mbox{C}_{6}\mbox{H}_{6}+\mbox{CH}_{4}$
4. Senyawa di bawah ini memiliki 4 cincin aromatik. Urutkan mereka berdasarkan kenaikan reaktivitas terhadap reaksi substitusi elektrofilik!

Jawaban
Kita beri kode searah jarum jam dari cincin di kiri atas (terikat dengan N) sebagai A , B, C, D.
Cincin A paling reaktif terhadap reaksi substitusi elektrofilik karena PEB milik N mengaktivasi cincin tersebut.
Cincin B tergolong gugus pendeaktivasi
Cincin C diaktivasi oleh gugus -OCO-R, namun tidak sekuat cincin A
Cincin D diaktivasi oleh gugus alkil, namun tergolong aktivator terlemah.
Sehingga urutannya berdasarkan kenaikan reaktivitas :
C, D, B, A



