Kalau kamu ingin belajar Kimia Kuantum secara lebih mendalam, coba simak penjelasan yang ada di sini. Setelah menerima materi, kamu bisa langsung mempraktikkannya dengan mengerjakan latihan soal yang telah kami sediakan.
Lewat pembahasan ini, kamu bisa belajar mengenai Kimia Kuantum. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Kimia Kuantum dalam bentuk pdf pada link dibawah ini:
Definisi
Aplikasi mekanika kuantum pada kimia yang digunakan untuk memahami dan memprediksi struktur, sifat dan mekanisme reaksi dari berbagai bahan.
Persamaan Gelombang
Persamaan dasar untuk gelombang digunakan untuk menemukan persamaan fundamental dari mekanika kuantum.
Suatu gelombang secara umum dinyatakan dalam persamaan gelombang sinus berikut:
$\psi(x,t)=A\sin2\pi\left(\frac{x}{\lambda}-\frac{t}{T}\right)$
dimana,
$\psi=$ perpindahan pada posisi x dan waktu t
$A=$ amplitudo
$T=$ frekuensi
$\lambda=$ panjang gelombang
Penurunan persamaan gelombang untuk gelombang elektromagnetik atau cahaya menghasilkan persamaan fundamental berikut:
$c=v\lambda$, dimana
$c=$ kecepatan cahaya
$v=$ frekuensi cahaya
$\lambda=$ panjang gelombang
Teori Kuantum untuk energi
Fenomena pemancaran cahaya (gelombang elektromagnetik) dari suatu bahan yang dipanaskan pada suhu tinggi, seperti pada besi dalam sebuah tungku atau elemen pemanas pada kompor listrik dikenal sebagai radiasi termal.
Radiasi termal dari sebuah benda hitam di mana benda hitam adalah sebuah contoh ideal tidak terjadinya pemantulan cahaya dan fenomena radiasi ini disebut sebagai radiasi benda hitam.
Pengukuran spektroskopi terhadap intensitas gelombang elektromagnetik yang dipancarkan sebagai fungsi panjang gelombang, $\lambda$ atau frekuensi $\nu$ menghasilkan bentuk karakteristik dari spektra tersebut.
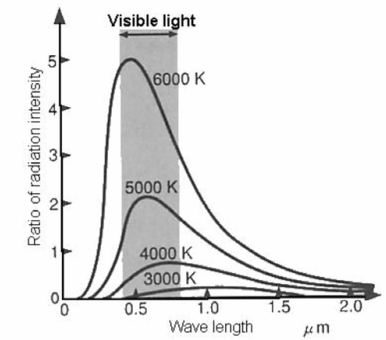
Spektra radiasi benda hitam pada suatu temperatur menunjukkan karakteristik tertentu dan perubahan bentuknya sangat bergantung pada temperatur dan ini dapat dilihat pada Gambar di bawah.
Panjang gelombang pada titik maksimum, $\lambda$ maks bergeser menuju panjang gelombang pendek jika temperatur absolutnya dinaikkan. Perkalian antara $\lambda$ maks dengan T adalah mendekati konstan. Fenomena ini dikenal sebagai hukum pergeseran Wien.
Pada tahun 1900, Planck berhasil memperkenalkan sebuah konsep baru tentang sebuah kuantum energi yang menghasilkan perumusan yang dapat menjelaskan radiasi termal.
Teori Planck ini memasukkan sebuah unit energi elementer yang berbanding lurus dengan frekuensi, $\nu$ untuk setiap osilator dan mengijinkan energi dari osilator ini untuk diasumsikan sebagai perkalian bilangan bulat dari frekuensi $\nu$ dan ditulis $nh\nu$.
Ini adalah jumlah satuan energi minimum $h\nu$ yang disebut sebagai kuantum energi dan h adalah konstanta Planck. Hasil eksperimen memberikan nilai h sebesar $h=6.6262\times10^{-34}$ .
$E=hv$
Dualisme Partikel-Gelombang
Pada tahun 1923, de Broglie mempostulasikan bahwa sebuah partikel dapat memiliki panjang gelombang yang berkaitan dengan momentum yang ia miliki melalui persamaan di mana momentum dan panjang gelombang adalah saling berhubungan satu dengan yang lainnya dan sebaliknya.
Sifat gelombang dari sebuah elektron disebut sebagai gelombang elektron dan secara umum sifat gelombang dari materi disebut sebagai gelombang materi atau gelombang de Broglie. Panjang gelombang $\lambda$ untuk gelombang materi diberikan oleh persamaan berikut, di mana juga ekivalen dengan persamaan
$\lambda=\frac{h}{p}$
dimana
$h=$konstanta Planck
$p=$momentum linear foton
Persamaan Schrodinger
Pada tahun 1926, persamaan dasar yang secara inklusif menyatakan sifat partikel dan gelombang diusulkan dalam kerangka mekanika gelombang oleh Schrodinger dan mekanika matriks oleh Heisenberg. Meskipun bentuk matematika yang diusulkan oleh mereka berbeda, teori ini dibuktikan memiliki kesamaan dalam pengertian fisika yang sangat penting oleh E. Schrodinger.
Berikut ini adalah persamaan Schrodinger:
$ih\frac{\partial\Psi}{\partial t}=\hat{H}\Psi$
Probabilitas untuk menemukan sebuah partikel yang bergerak sepanjang sumbu x pada suatu daerah tertentu antara x dan x + dx dinyatakan sebagai $|\Psi(x,t)|^{2}dx$ dengan menggunakan fungsi gelombang $\Psi(x,t)$ Karena probabilitas untuk menemukan partikel pada daerah antara $x=-\infty$ hingga $x=+\infty$ adalah sama dengan 1, maka integral berikut harus sama dengan 1.
$\int_{-\infty}^{\infty}|\Psi(x,t)^{2}|dx=1$
Ini disebut sebagai kondisi renormalisasi dari sebuah fungsi gelombang. Jika kondisi ini dipenuhi, maka fungsi gelombang tersebut dikatakan ternormalisasi.
Partikel dalam Kotak Satu Dimensi
Fungsi gelombang dengan bilangan kuantum n dalam sebuah kotak ( 0 < x < L) dengan panjang L diberikan oleh persamaan
$\Psi_{n}(x)=\sqrt{\frac{2}{L}}\sin\left(\frac{n\pi x}{L}\right)$ $(n=1,2,3,…)$, tingkat energi
Contoh Soal Kimia Kuantum dan Pembahasannya
1. Tunjukkanlah hubungan berikut akan terjadi diantara fungsi gelombang $\psi_{n}(x)$ dan $\psi_{m}(x)$ untuk sebuah partikel dalam kotak satu dimensi.
$\int_{-\infty}^{\infty}\psi_{n}(x)^{*}\psi_{m}(x)dx=\delta_{nm}$
$\delta_{nm}$ adalah delta Kronecker dimana akan sama dengan 1 jika $n=m$ dan 0 jika $n\neq m$
Jawaban
Ingat bahwa fungsi gelombang dengan bilangan kuantum n dalam sebuah kotak ( 0 < x < L) dengan panjang L diberikan oleh persamaan
$\Psi_{n}(x)=\sqrt{\frac{2}{L}}\sin\left(\frac{n\pi x}{L}\right)$,
Untuk posisi di luar kotak, kita sebut integral yang menjadi masalah sebagai $I_{nm}$:
$I_{nm}=\int_{0}^{L}\left(\frac{2}{L}\right)\sin\left(\frac{n\pi x}{L}\right)\sin\left(\frac{m\pi x}{L}\right)dx$
Sesuai rumus trigonometri:
$\sin A\sin B=\frac{1}{2}(\cos(A-B)-\cos(A+B))$
Dengan demikian:
$I(\pm)=\left(\frac{1}{L}\right)\int_{0}^{L}\cos\left(\frac{(n\pm)\pi x}{L}\right)dx$
Dengan menuliskan $\theta=\frac{\pi x}{L}$ maka diperoleh
$I(\pm)=\left(\frac{1}{\pi}\right)\int_{0}^{\pi}\cos\left(n\pm m\right)\theta d\theta$
Ketika $\left(n\pm m\right)$ tidak sama dengan 0,
$I(\pm)=\left[\frac{1}{\pi}\left\{ \frac{1}{n\pm m}\right\} \sin\left(n\pm m\right)\theta\right]_{0}^{\pi}=0$
Ketika $n=m$ ($n-m=0$) ,
$\begin{aligned}I(-) & =\frac{1}{\pi}\int_{0}^{\pi}d\theta\\ & =\frac{\pi}{\pi}\\ & =1 \end{aligned} $
Maka,
(a) Untuk $n=m$, $I_{nm}=1$
(b) Untuk $n\neq m$, $I_{nm}=0$, dengan delta Kronecker kita akan memperoleh $I_{nm}=\delta_{nm}$


