Ingin mempelajari Atom Hidrogen secara lebih mendalam? Kamu bisa menyimak baik-baik pembahasan yang ada di sini. Setelahnya, kamu bisa mengerjakan kuis berupa latihan soal untuk mengasah kemampuan.
Lewat pembahasan ini, kamu bisa belajar mengenai Atom Hidrogen. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Atom Hidrogen dalam bentuk pdf pada link dibawah ini:
Definisi
Rentetan warna diskontinu yang diperoleh apabila cahaya dari eksitasi atom hidrogen diuraikan ke dalam komponennya.
Spektrum Atom Hidrogen
Suatu spektrum (atau spektra) atau rentetan warna yang terlihat oleh kita sehari-hari biasanya merupakan suatu spektra kontinu karena terdiri atas banyak komponen dengan panjang gelombang masing-masing.
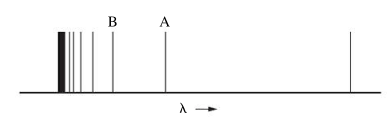
Sementara itu, apabila sumber spektrum hanya menghasilkan sedikit komponen panjang gelombang, maka akan terbentuk spektrum diskontinu, seperti yang diamati pada spektrum hidrogen, yang terlihat pada gambar sebagai berikut.
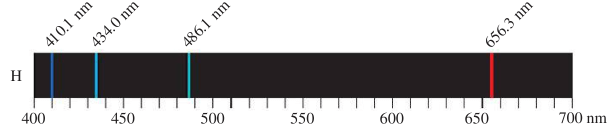
Berdasarkan spektra ini Johann Balmer mengemukakan persamaan sebagai berikut:
$v=3,2881\times10^{15}s^{-1}\left(\frac{1}{2^{2}}-\frac{1}{n^{2}}\right)$
dimana,
$v=$frekuensi garis spektra
$n=$suatu bilangan bulat yang lebih besar dari 2.
Bila kita masukkan $n=3$, didapat frekuensi yang sesuai dengan garis merah, bila $n=4$ didapat frekuensi garis hijau dan seterusnya.
Teori fisika klasik tidak dapat menjelaskan terbentuknya spektrum atom ini, maka dimulailah era teori kuantum.
Menggunakan teori kuantum yang dikemukakan Max Planck dan beberapa prinsip fisika klasik Niels Bohr mengemukakan teori atomnya dan perhitungan tingkat energi elektron pada suatu orbit $n$, sebagai:
$E_{n}=\frac{-R_{H}}{n^{2}}$
dimana
$E_{n}=$tingkat energi atom pada orbit $n$
$R_{H}=$konstanta Rydberg untuk atom Hidrogen, $2,179\times10^{-18}$J
Normalnya pada atom hidrogen, elektron berada pada tingkat dasar (ground state) dengan $n=1$, dan ketika elektron ini menerima satu kuanta energi (paket energi) ia dapat berpindah ke tingkat energi yang lebih tinggi ($n=2,3,$ dan seterusnya).
Sebaliknya ketika elektron dari tingkat energi tertentu kembali ke tingkat dasar maka ia akan mengemisikan energi dalam bentuk foton dengan energi sebesar selisih antara kedua tingkat energi tersebut. Maka, didapat:
$\begin{aligned}\Delta E & =hv\\ R_{H}\left(\frac{1}{n_{i}^{2}}-\frac{1}{n_{f}^{2}}\right) & =hv \end{aligned} $
dimana,
$n_{i}=$ tingkat energi awal (\emph{initial}) sebelum transisi elektron
$n_{f}=$ tingkat energi akhir (\emph{final}) setelah transisi elektron
$h=$ konstanta Planck ($6,626\times10^{-34}m^{2}kg/s$)
$v=$ frekuensi foton yang diemisikan
Ingat pada perhitungan panjang gelombang atau frekuensi foton yang akan diabsorbsi atau diemisikan nilai negatif dapat diabaikan, karena nilai negatif disini hanya melambangkan perbedaan tingkat energi.
Selain untuk hidrogen, teori Bohr dapat diaplikasikan untuk spesi-spesi yang mirip hidrogen, seperti $He^{+}$ dan $Li^{2+}$ yang digambarkan melalui persamaan:
$E_{n}=\frac{-Z^{2}R_{H}}{n^{2}}$
dimana,
$Z=$ nomor atom unsur
Selain itu teori Bohr juga dapat memprediksi jari-jari suatu orbit atom hidrogen melalui persamaan:
$r_{n}=n^{2}a_{0}$
dimana,
$r_{n}=$jari-jari orbit atom hidrogen pada tingkat energi tertentu
$a_{0}=$jari-jari Bohr / jari-jari pada tingkat dasar, yakni 53 pm
Nilai $a_{0}$ ini didapat dari persamaan
$a_{0}=\frac{4\pi\epsilon_{0}\hbar^{2}}{m_{e}e^{2}}$
$a_{0}=$ radius atom Bohr
$\epsilon_{0}=$ permitivitas
$\hbar=$ $\frac{h}{2\pi}$ dimana h adalah konstanta Planck
$m_{e}=$ massa elektron
$e=$ muatan elektron
Deret Spektra Atom Hidrogen
Berbagai spektra atom hidrogen yang ditemukan disusun ke dalam deret-deret berikut:
- Deret Lyman ($n_{f}=1$) dihasilkan dari transisi elektron ke tingkat dasar mulai dari $n=\infty$ hingga $n=2$
- Deret Balmer ($n_{f}=2$) dihasilkan dari transisi elektron ke tingkat energi kedua
- Deret Paschen ($n_{f}=3$)
- Deret Brackett ($n_{f}=4$)
- Deret Pfund ($n_{f}=5$)
Contoh Soal dan Pembahasan
- Tentukan warna yang mungkin timbul bila terjadi transisi dari $n=5$ ke $n=3$ pada ion $Be^{3+}$!
Jawaban
$\begin{aligned}\Delta E & =RZ^{2}\frac{1}{n_{i}^{2}}-\frac{1}{n_{f}^{2}}\\ \frac{hc}{\lambda} & =2,179\times10^{-18}\times4^{2}\left(\frac{1}{5^{2}}-\frac{1}{3^{2}}\right)\\ \frac{1,986\times10^{-25}}{\lambda} & =2,479\times10^{-18}\\ \lambda & =0,80113\times10^{-7}m\\ & =80,113nm \end{aligned}$ (nilai negatif dapat diabaikan).
Foton yang diemisikan berada di bawah panjang gelombang visible, maka tidak akan ada cahaya yang nampak.