Kalau kamu ingin mempelajari pembahasan tentang Teori Orbital Molekul, simak penjelasan lengkapnya di sini. Setelah mempelajari materinya, kamu bisa mengerjakan soal-soal latihan yang telah disediakan.
Lewat pembahasan ini, kamu bisa belajar mengenai Teori Orbital Molekul. kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal teori orbital molekul pdf pada link dibawah ini:
Definisi
Pengertian teori orbital molekul (molecular orbital theory) adalah merupakan teori yang menjelaskan bagaimana tumpang tindih dan penggabungan orbital atom pada molekul.
Teori Orbital Molekul
Dalam molecular orbital terdapat 2 orbital yang dengan nama orbital bonding dan anti-bonding. Orbital molekul bonding adalah orbital dengan rapatan elektron ikatan terpusat mendekat pada daerah antara kedua inti atom yang bergabung dan akan lebih stabil.
Pengertian orbital molekul anti-bonding adalah orbital rapatan elektron ikatan terpusat yang menjauh dari daerah antara inti atom yang bergabung dan bersifat kurang stabil.
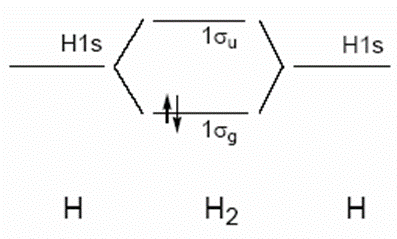
1. Diagram orbital molekul $\mbox{H}_{2}$

2. Diagram orbital molekul $\mbox{N}_{2}$ dan $\mbox{O}_{2}$


3. Orde Ikatan
Dalam molecular orbital theory, kestabilan ikatan kovalen berhubungan dengan orde ikatan. Jika nilai orde ikatan lebih besar dari 0, berarti molekul tersebut stabil sedangkan jika nilai orde ikatan sama dengan 0, maka molekul tersebut tidak stabil.
Orde ikatan sebanding dengan ukuran stabilitas termal.$\mbox{orde ikatan}=\frac{\sum elektron\, ikatan-\sum elektron\, anti\, ikatan}{2}$
Contoh menentukan orde ikatan pada $\mbox{O}_{2}$

$\begin{alignedat}{1}\mbox{orde ikatan }\mbox{O}_{2} & =\frac{10-6}{2}\\
& =2
\end{alignedat}
$
Contoh Soal dan Pembahasan
Terdapat spesi $\mbox{N}_{2}$ dan $\mbox{O}_{2}^{+}$
- Manakah yang lebih stabil antara $\mbox{N}_{2}$ atau $\mbox{O}_{2}^{+}$ ? Jelaskan!
- Manakah yang merupakan spesi paramagnetik?
- Tuliskan konfigurasi elektron ion $\mbox{O}_{2}^{+}$ tersebut dalam konteks orbital molekul (molecular orbital)!
Jawaban
-
- menggambarkan orbital molekul $\mbox{N}_{2}$
$_{7}\mbox{N}:1s^{2}2s^{2}2p^{3}$

menggambarkan molecular orbital $\mbox{O}_{2}^{+}$
$_{8}\mbox{O}:1s^{2}2s^{2}2p^{4}$

Kestabilan dapat dilihat dari nilai orde ikatannya,
Orde ikatan $\mbox{N}_{2}=\frac{10-6}{2}=2$Orde ikatan $\mbox{O}_{2}^{+}=\frac{10-5}{2}=2,5$
Karena orde ikatan $\mbox{O}_{2}^{+}>\mbox{N}_{2}$, maka $\mbox{O}_{2}^{+}$ lebih stabil. - Sifat paramagnetik dikarenakan adanya elektron yang tidak berpasangan. Dari diagram molecular orbital, dapat dilihat bahwa $\mbox{O}_{2}^{+}$ mempunyai elektron tidak berpasangan sedangkan pada $\mbox{N}_{2}$, semua elektronnya berpasangan semua. Sehingga $\mbox{O}_{2}^{+}$ yang mempunyai sifat paramaagnetik.
- konfigurasi elektron ion $\mbox{O}_{2}^{+}$: $(\sigma_{1s})^{2}(\sigma_{1s}^{*})^{2}(\sigma_{2s})^{2}(\sigma_{2s}^{*})^{2}(\sigma_{2pz})^{2}(\pi_{2p})^{4}(\pi_{2p}^{*})^{1}$
- menggambarkan orbital molekul $\mbox{N}_{2}$